第 661 期 2016-08-05
知識產權 新藥再創新猷—漫談2015年美國FDA核准小分子新藥(下)
Introduction to FDA approved novel small molecular drugs in 2015 (part 3) 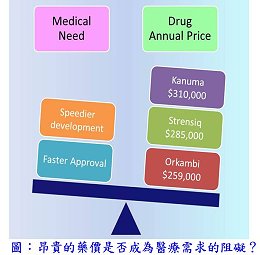 隨著審查效能的提升,藥物自研發到獲得核准的時程已有效縮短,對患者而言,實是一大福音;然而,高單價卻也引發另一個無法承擔之重,2015年獲核准之新藥中有12個藥物之藥價1年高於10萬美元[註1]。本期介紹的9個新藥當中有3個(Cholbam® 、Orkambi® 和Xuriden® )是用於治療患者總數少於20萬人的罕見疾病藥物,當中的Xuriden® 更是被用於超級罕見疾病(ultra-rare disease)—遺傳性乳清酸尿症(hereditary orotic aciduria)的治療,全世界僅有約二十名患者,而Orkambi® 則是2015年獲核准新藥中的第三高藥價,1年需25.9萬美元。〈更多內容〉
隨著審查效能的提升,藥物自研發到獲得核准的時程已有效縮短,對患者而言,實是一大福音;然而,高單價卻也引發另一個無法承擔之重,2015年獲核准之新藥中有12個藥物之藥價1年高於10萬美元[註1]。本期介紹的9個新藥當中有3個(Cholbam® 、Orkambi® 和Xuriden® )是用於治療患者總數少於20萬人的罕見疾病藥物,當中的Xuriden® 更是被用於超級罕見疾病(ultra-rare disease)—遺傳性乳清酸尿症(hereditary orotic aciduria)的治療,全世界僅有約二十名患者,而Orkambi® 則是2015年獲核准新藥中的第三高藥價,1年需25.9萬美元。〈更多內容〉
《文/圖:生技與藥物研究所謝興邦研究員、李靜琪副研究員;審校:生技與藥物研究所陳炯東研究員》



