NHRI Communications

研究發展
以KRAS突變與否進行隨機分組的第II期臨床試驗:探討單獨使用化療或化療加上表皮生長因子受體抗體為第一線治療不可切除局部晚期性或轉移性之膽道癌
A KRAS mutation status-stratified randomized phase II trial of gemcitabine and oxaliplatin alone or in combination with cetuximab in biliary tract cancer
 與西方國家相比,台灣膽道癌的發生機率相對而言較高,且預後並不理想。鑒於晚期膽道癌之治療缺乏有效之化學治療藥物,本院癌症研究所姜乃榕醫師與陳立宗所長之研究團隊於「臺灣癌症臨床研究合作組織(TCOG)」 提出針對膽道癌的臨床試驗。Gemcitabine和oxaliplatin之複方化療可便於門診施打,其副作用也相對輕微且為患者接受。此外,超過80%的膽管癌有表皮生長因子(epidermal growth factor receptor, EGFR)的過度表現,而愛必妥(Erbitux ®(cetuximab))是一個表皮生長因子受體抗體,可以拮抗EGFR,進而阻止細胞訊息傳遞。另外從大腸直腸癌的治療經驗顯示,KRAS若有突變將對cetuximab的治療沒有反應;因此在本試驗中,研究團隊將以KRAS突變與否隨機分組第II期臨床試驗,探討gemcitabine和oxaliplatin之複方化療(GEMOX)單獨使用或合併cetuximab(C-GEMOX)在不可切除局部晚期或轉移性膽道癌患者的療效及毒性,並在試驗後分析KRAS突變與否對治療效果的影響。
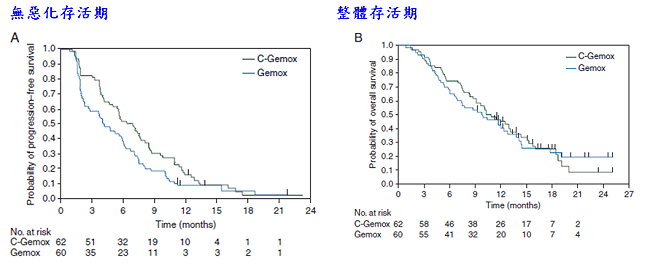
與西方國家相比,台灣膽道癌的發生機率相對而言較高,且預後並不理想。鑒於晚期膽道癌之治療缺乏有效之化學治療藥物,本院癌症研究所姜乃榕醫師與陳立宗所長之研究團隊於「臺灣癌症臨床研究合作組織(TCOG)」 提出針對膽道癌的臨床試驗。Gemcitabine和oxaliplatin之複方化療可便於門診施打,其副作用也相對輕微且為患者接受。此外,超過80%的膽管癌有表皮生長因子(epidermal growth factor receptor, EGFR)的過度表現,而愛必妥(Erbitux ®(cetuximab))是一個表皮生長因子受體抗體,可以拮抗EGFR,進而阻止細胞訊息傳遞。另外從大腸直腸癌的治療經驗顯示,KRAS若有突變將對cetuximab的治療沒有反應;因此在本試驗中,研究團隊將以KRAS突變與否隨機分組第II期臨床試驗,探討gemcitabine和oxaliplatin之複方化療(GEMOX)單獨使用或合併cetuximab(C-GEMOX)在不可切除局部晚期或轉移性膽道癌患者的療效及毒性,並在試驗後分析KRAS突變與否對治療效果的影響。Gemcitabine、oxaliplatin和cetuximab皆為兩週施打1次,會持續治療直到腫瘤進展、患者無法耐受或腫瘤縮小至可以開刀才停止。此計畫自2010年12月開始收案,到2012年5月結束收案,共有122位受試者(60位患者接受GEMOX;62位患者接受C-GEMOX)。接受C-GEMOX治療的患者較接受GEMOX治療的患者有較長的治療時間(中位數:4.9 vs. 3.0 個月; p = 0.01)、較高的整體反應率(27% vs. 15%; p = 0.12)和疾病控制率(58% vs. 37%; p = 0.02)及較長的無惡化存活期(PFS: 6.7 vs. 4.1 個月; p = 0.05),但兩群的整體存活期是相近的(OS: 10.6 vs. 9.8 個月; p = 0.91)。兩組患者的副作用發生率大致上類似,但皮疹、過敏反應及嗜中性白血球低下則是在C-GEMOX組較常見。接受C-GEMOX治療後,有發生較嚴重皮疹(相較於只有輕微或沒有發生皮疹的患者)、有顯著較好的反應率、無惡化存活期和整體存活期。36%的腫瘤有KRAS突變,但有無此突變病並不會影響患者接受GEMOX或C-GEMOX的效果。在試驗後也針對腫瘤其他的突變點,例如NRA和BRAF(V600E)進行分析,結果顯示有9個腫瘤有NRAS突變及沒有腫瘤有BRAF突變,有無RAS (KRAS + NRAS)突變對患者接受GEMOX或C-GEMOX的預後也不會有影響。
將cetuximab加入gemcitabine和oxaliplatin治療膽道癌雖然無法延長整體存活率,但會有較好的疾病控制率和無惡化存活期,且副作用是可以接受的;使用cetuximab後有產生皮疹副作用的患者,則會有較好的反應率和較長的存活期。此計畫將是表皮生長因子受體抗體使用於亞洲膽道癌病患者之唯一隨機分組的臨床試驗,且所有研究計畫中使用之cetuximab、gemcitabine及oxaliplatin均無健保給付,而由研究者以起始計畫(investigator-initiated project)方式向廠商申請,無償提供受試者使用。此計畫約一年半就收滿100多位患者,顯示台灣膽道癌患者人數比想像中多,且有意願參加臨床試驗期獲得更多的治療機會,相信藥物臨床試驗在膽道癌方面大有可為。此臨床試驗結果已發表於Annals of Oncology (2015;26(5): 943-949)。
《文/圖:癌症研究所姜乃榕醫師、陳立宗所長》