NHRI Communications

研究發展
幹細胞特性可藉由幹細胞胞外體(SC-exosomes)轉移,開啟再生醫學新方向
NHRI researchers report stem cell states can be transferred via stem cell-derived exosomes, proposing a new direction for regenerative medicine
 近年來,幹細胞之研究及應用為科學上眾所注目的焦點之一,幹細胞的臨床應用也為再生醫學帶來了一線曙光。然而現今幹細胞分化的功能尚未完全釐清,再加上幹細胞取得不易、數量稀少,以及培養困難等因素,使得現今幹細胞治療上,存在許多風險及困難度。因此,針對幹細胞生理及其分化機制的相關研究,對再生醫學具有莫大助益。
近年來,幹細胞之研究及應用為科學上眾所注目的焦點之一,幹細胞的臨床應用也為再生醫學帶來了一線曙光。然而現今幹細胞分化的功能尚未完全釐清,再加上幹細胞取得不易、數量稀少,以及培養困難等因素,使得現今幹細胞治療上,存在許多風險及困難度。因此,針對幹細胞生理及其分化機制的相關研究,對再生醫學具有莫大助益。前列腺素E2(prostaglandin E2)訊號傳遞對於維持體內幹細胞恆定扮演非常重要的角色,於幹細胞自我更新及再生上亦不可或缺,但其中重要的分子機制至今仍然尚未釐清。本院細胞及系統醫學研究所李華容助研究員與林孟杰博士後研究員等人發現,阻斷乳腺幹細胞之前列腺素E2訊號傳遞可促使維持幹細胞特性之分子聚集於細胞膜的脂筏(lipid-raft)內。這些含幹細胞特性分子之脂筏更進一步地經由胞外體(exosomes)大量被釋放至細胞外(圖一),進而導致乳腺幹細胞失去其幹細胞特性,分化形成乳腺上皮細胞。研究團隊也發現,這些被誘發的幹細胞胞外體(stem cell-derived exosomes, SC-exosomes)可被已分化的乳腺上皮細胞吞噬,促使已分化的細胞重獲幹細胞特性(圖一)。另一方面,團隊也利用此誘發的幹細胞胞外體,成功地轉化已分化的乳腺管腔細胞為乳腺幹細胞,並能用於動物體內,重建乳腺組織(圖二)。
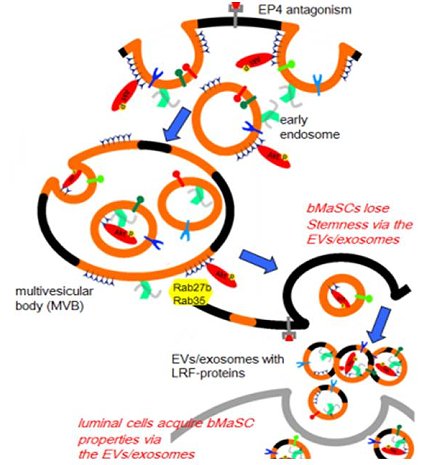
圖一:前列腺素E2訊號傳遞路徑被阻斷的情況之下,幹細胞大量釋放胞外體。此胞外體可被已分化的細胞吞噬,促使其重獲幹細胞特性。
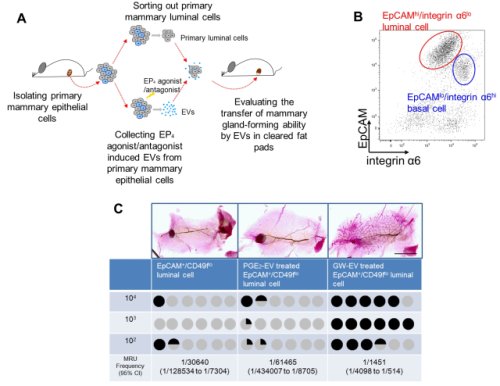
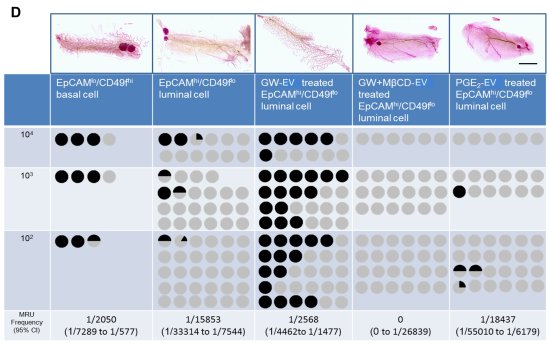
圖二:團隊成功利用產生的胞外體誘發幹細胞,並於動物體內重建乳腺組織。
此項研究有助於瞭解前列腺素E2之訊號傳遞於幹細胞分化上的分子機制,並且證實幹細胞特性可藉由胞外體於細胞之間進行轉移。此研究成果於發展非細胞性幹細胞胞外體之治療與應用具有極大的潛力,是再生醫學上的重大突破。目前,研究團隊以此研究結果為方向,積極尋求多種幹細胞胞外體於組織再生上之應用。相關研究成果已申請專利,並於8月發表在Stem Cells期刊(in press; DOI: 10.1002/stem.2476)。
《文/圖:細胞及系統醫學研究所李華容助研究員、林孟杰博士後研究員》