NHRI Communications

研究發展
多功能性中孔洞奈米矽球用於體內追蹤與光動力治療之研究現況
Functionalization of Mesoporous Silica Nanoparticles for In Vivo Optical Imaging and Photodynamic Therapy: Current Status
 奈米科技在生物醫學的應用在近年來引起了廣泛的研究與討論。利用奈米科技除了可以提供靶向傳遞與藥物控釋的功能外,另一個重要的特點乃在於可以同時兼具體內追蹤的功能。最近由本院醫學工程研究組羅履維副研究員、奈米醫學中心楊重熙主任與台灣大學化學系牟中原教授此研究團隊共同研發出一系列以奈米矽球為載體之多功能智慧型傳遞系統。由於奈米矽球具備極高的內表面積、規則性孔洞排列與表面基團容易被活化等特性,因此可被利用來吸附、捕捉、或修飾上大量之生物分子、螢光物質或藥物分子。先前本研究團隊已闡述了利用奈米矽球作為口服結腸定位釋藥載體 (Adv. Funct. Mater.2008, 18, 3283.),本文將進一步介紹奈米矽球作為體內追蹤與光動力治療之研究現況。
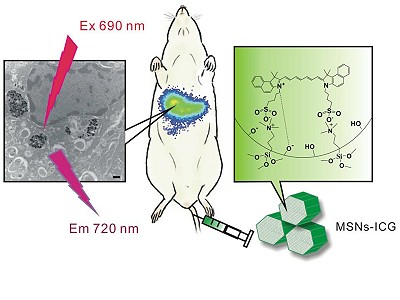
奈米科技在生物醫學的應用在近年來引起了廣泛的研究與討論。利用奈米科技除了可以提供靶向傳遞與藥物控釋的功能外,另一個重要的特點乃在於可以同時兼具體內追蹤的功能。最近由本院醫學工程研究組羅履維副研究員、奈米醫學中心楊重熙主任與台灣大學化學系牟中原教授此研究團隊共同研發出一系列以奈米矽球為載體之多功能智慧型傳遞系統。由於奈米矽球具備極高的內表面積、規則性孔洞排列與表面基團容易被活化等特性,因此可被利用來吸附、捕捉、或修飾上大量之生物分子、螢光物質或藥物分子。先前本研究團隊已闡述了利用奈米矽球作為口服結腸定位釋藥載體 (Adv. Funct. Mater.2008, 18, 3283.),本文將進一步介紹奈米矽球作為體內追蹤與光動力治療之研究現況。ICG(indocyanine green)是FDA核可並可用於人體之近紅外光區螢光顯影劑。由於其激光與放光皆在長波長光區,而大部分的生物分子在此光區並無吸收與放光的現象,因此可以大量降低背景值的干擾。然而,ICG作為一螢光顯影劑受到一些限制,例如:ICG分子在光、熱、酸或鹼性的作用下易造成分解;在生理溶液中ICG易產生聚集現象而喪失螢光;ICG容易與蛋白質高度的結合(大約95%的ICG),在體內很快速的被移除並分解。因此,利用奈米矽球可將ICG分子良好的保護在其孔洞內,可以有效解決以上所面臨的問題,並產生一高效率的螢光作為生物體內有效之光學訊號放大器。此技術不但可發展用來快速評估奈米粒子在體內的靶向與生物分佈,可進一步被用來追蹤並確認病灶。此部分研究結果,已被國際期刊Adv. Funct. Mater. 所接受﹝SCI = 7.496﹞。
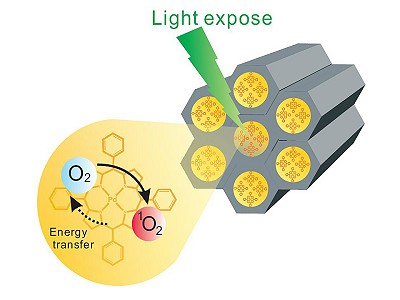 另一方面我們利用奈米載體中孔洞奈米矽球附載鈀紫質(Pd-meso-tetra(4-carboxyphenyl) porphyrin (PdTPP) )來對於MDA-MB-231乳癌細胞進行光動力療法(Photodynamic therapy, PDT)。光動力療法是利用特定波長的雷射,照射光敏試劑(Photosensitizer)使其受到激發,而激發態的光敏試劑將能量傳遞給周圍的氧,生成活性很強的單重態氧(1O2),單重態氧和相鄰的生物分子發生氧化反應,會産生細胞毒性作用,進而導致細胞受損乃至死亡。由於光動力療法與周遭氧氣濃度關聯性極高,然而鈀紫質同時具有量測周遭氧分子濃度,以及其高單重態氧氣光轉換效率的特性,因此選擇鈀紫質做為光敏試劑,可以進而達到同步診斷及治療的目標。我們運用中孔洞奈米矽球表面積極高的特性,以共價鍵在孔洞內大量修飾鈀紫質來提高光敏劑量的單位濃度,且中孔洞奈米矽球容易被細胞所吞噬,使得我們得以較低的激發能量即可達到高細胞毒殺的能力。此PDT相關的研究計畫由國家衛生研究院醫學工程研究組羅履維副研究員、奈米醫學中心楊重熙主任、清華大學工科系曾繁根教授與台灣大學化學系牟中原教授共同合作,研究成果也已被國際期刊J. Mater. Chem.﹝SCI = 4.34﹞接受。
另一方面我們利用奈米載體中孔洞奈米矽球附載鈀紫質(Pd-meso-tetra(4-carboxyphenyl) porphyrin (PdTPP) )來對於MDA-MB-231乳癌細胞進行光動力療法(Photodynamic therapy, PDT)。光動力療法是利用特定波長的雷射,照射光敏試劑(Photosensitizer)使其受到激發,而激發態的光敏試劑將能量傳遞給周圍的氧,生成活性很強的單重態氧(1O2),單重態氧和相鄰的生物分子發生氧化反應,會産生細胞毒性作用,進而導致細胞受損乃至死亡。由於光動力療法與周遭氧氣濃度關聯性極高,然而鈀紫質同時具有量測周遭氧分子濃度,以及其高單重態氧氣光轉換效率的特性,因此選擇鈀紫質做為光敏試劑,可以進而達到同步診斷及治療的目標。我們運用中孔洞奈米矽球表面積極高的特性,以共價鍵在孔洞內大量修飾鈀紫質來提高光敏劑量的單位濃度,且中孔洞奈米矽球容易被細胞所吞噬,使得我們得以較低的激發能量即可達到高細胞毒殺的能力。此PDT相關的研究計畫由國家衛生研究院醫學工程研究組羅履維副研究員、奈米醫學中心楊重熙主任、清華大學工科系曾繁根教授與台灣大學化學系牟中原教授共同合作,研究成果也已被國際期刊J. Mater. Chem.﹝SCI = 4.34﹞接受。《文/圖:醫學工程研究組程士勳博士班研究生、羅履維副研究員;奈米醫學研究中心李佳洪博士後研究員》