NHRI Communications

院務紀事
生技與藥物研究所正式成立
Establishment of Institute of Biotechnology and Pharmaceutical Research at NHRI
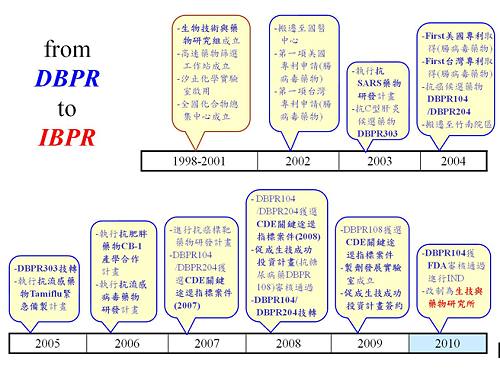 本院「生技與藥物研究所」(Institute of Biotechnology and Pharmaceutical Research, IBPR)於2010年8月11日正式成立,前身為生物技術與藥物研究組(設立於1998年1月)。歷年來該組所建置之整合性新藥研發團隊已進行包括癌症、新陳代謝疾病及病毒感染症等三大領域疾病新穎治療藥物的開發與研究。所建立之整合性新藥研究設施與技術包括分子生物、藥物化學合成、分子結構模擬、自動化高速藥物篩選、動物藥理、藥物動力與藥物代謝,以及分析與配方製劑研究實驗室等,已臻完備,是國內唯一由政府經費支持,且具有完整新藥上游研究技術平台的研究單位。
本院「生技與藥物研究所」(Institute of Biotechnology and Pharmaceutical Research, IBPR)於2010年8月11日正式成立,前身為生物技術與藥物研究組(設立於1998年1月)。歷年來該組所建置之整合性新藥研發團隊已進行包括癌症、新陳代謝疾病及病毒感染症等三大領域疾病新穎治療藥物的開發與研究。所建立之整合性新藥研究設施與技術包括分子生物、藥物化學合成、分子結構模擬、自動化高速藥物篩選、動物藥理、藥物動力與藥物代謝,以及分析與配方製劑研究實驗室等,已臻完備,是國內唯一由政府經費支持,且具有完整新藥上游研究技術平台的研究單位。近三年來,藉由與國內外委託研究機構(Contract Research Organization, CRO)的合作,將所研發出來的三項候選藥物(DBPR104, DBPR204, DBPR108)推動至中游的臨床前毒理發展階段,也積極進行藥物發展相關工作。此外,自2000年起參與及執行國科會「生技製藥國家型科技計畫」,經產學研合作與研發成果移轉兩大策略,與國內學術、研究機構及業界合作,進行新藥研發資源分享,並推動本院之藥物研發成果應用,卓然有成。例如DBPR104抗癌候選藥物,自2004年起進行一系列藥物開發試驗,並於2008年8月技術移轉給國內著名大藥廠—杏輝醫藥集團,進行後續新藥發展、製程開發與臨床試驗。經過旗下杏國生技持續戮力推動,已於今年7月30日通過美國食品藥物管理局(FDA)審查,准予進行第一期臨床試驗。此外刻正執行一項行政院「生技成功投資案例」計畫以及數項產學合作案。該研究團隊也曾參與多項衛生署重要衛生政策與議題,並配合緊急公共衛生需求執行重大專案研究計畫(例如抗SARS及流感藥物研發專案)。
本院為財團法人研究機構,執行上游階段研究工作,而在藥物研發領域,必須與研究發展鏈的中游研究機構及產業有所銜接,才能落實研究成果。因此,生技與藥物研究所將定位為以創新藥物的應用研究和應用開發為主的整合性藥物研究所,訂定之目標為:
1. 以應用開發為導向,進行整合性新藥研究,研發具專利新穎性的藥物與技術;
2. 推動產學研合作與技術移轉,落實新藥研發成果;
3. 建立具國際水準的新藥研究與發展技術平台,成為我國重要的創新藥物研究中心之一。
生技與藥物研究所將著重於「以專利新穎性為導向之藥物研發,並兼具國內需求及全球競爭性」。邀集跨領域之優秀專家,整合研發資源聚焦於利民與利基領域,建立完整的生技製藥研究發展體系,將研發成果產業化,以期產出具有創新性與前瞻性的新藥。研究方向為主要為1.治療癌症、新陳代謝疾病、病毒感染症、神經性疾病以及其他重要疾病的新藥探索(drug discovery);2.候選藥物之臨床前發展(drug development)。
一般新藥研發的過程在「非臨床階段」包括:
1. 藥物探索階段(Drug Discovery):
此階段通常要花數年建立適宜且有效的化合物篩選方法,研究活性化合物的作用機制與藥理,以確認其是否具開發的潛力。化合物經過結構設計以及化合物的修飾後,需進行小量試製(scale-up synthesis),並建立了快速合成新藥(New Molecular Entities, NMEs)的方法。一般來說,新藥探索階段約需2-10年。
2. 臨床前發展(Pre-clinical Development):
在新藥進行人體試驗前,必須先後以活體外實驗及活體內(動物)試驗,篩選其生物活性及安全性,並針對藥物動力及代謝、劑型配方、製程與安定性等進行評估。臨床前試驗的重要目的在於確認該藥品有足夠的生物活性以及評估藥品對人體是否有其他未知的副作用,以決定是否繼續投入時間及資金進行後續的臨床試驗。此階段為期2-4年。
生技與藥物研究所除了延續過去橫向的整合性新藥研發策略外,更將把上游新藥探索的研發成果,垂直連結至中游的臨床前發展,如下圖。
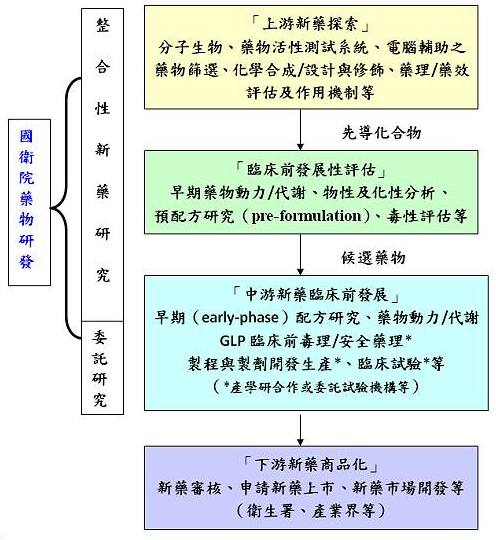
新藥之臨床前發展階段所需資金龐大,由於國內藥廠對新藥的臨床前發展缺乏足夠的經驗、人才與資金,且大部分廠商對投入「缺乏臨床前試驗資料之候選藥物」的研發信心不足,因此過去數年在新藥探索上雖陸續有研究成果產出,卻在技術移轉過程中遭遇困難。為解決此問題,並協助銜接國內新藥研發體系上、中游之發展,生技與藥物研究所在藥物研究之發展鏈將定位為上游新藥探索,並橋接至中游先期研究(臨床前發展)。
《文/圖:生技與藥物研究所》