NHRI Communications

健康知識
登革熱疫苗研發的進展與挑戰
Dengue vaccines: progress and challenges
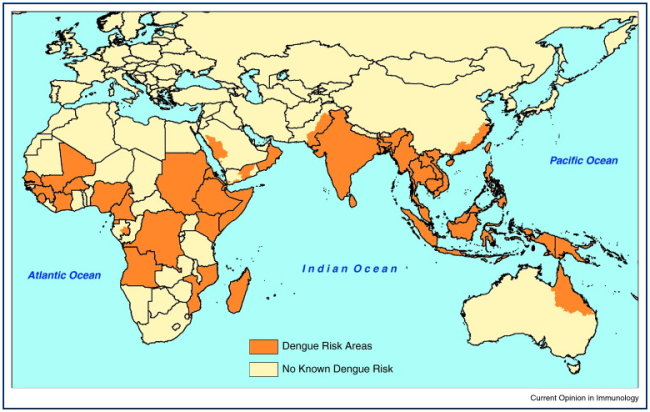
登革熱(Dengue fever, DF)主要流行在熱帶及亞熱帶地區,居住在這個地區的人口約25億人,佔全球人口40%。全世界每年感染登革熱約有5000萬到1億人、出血性登革熱病例50萬件、死亡病例已高達2萬2000件。
從最早有登革熱的研究報導迄今已超過50年,雖然科學家對登革病毒的特性漸漸有所瞭解,但是至今還沒有可用的疫苗上市,主要是因為登革熱有著多變的流行病學型態,不斷影響著疫苗的開發。
登革熱的病源為登革熱病毒,此病毒可分為4種登革熱病毒血清型。感染過一種登革熱病毒後,對該登革熱病毒會產生終生免疫,但對不同血清型的登革熱病毒則不太具有免疫效果。反而在接下來感染到不同型的登革熱時,可能引發更嚴重的出血性登革熱(Dengue hemorrhagic fever, DHF)。
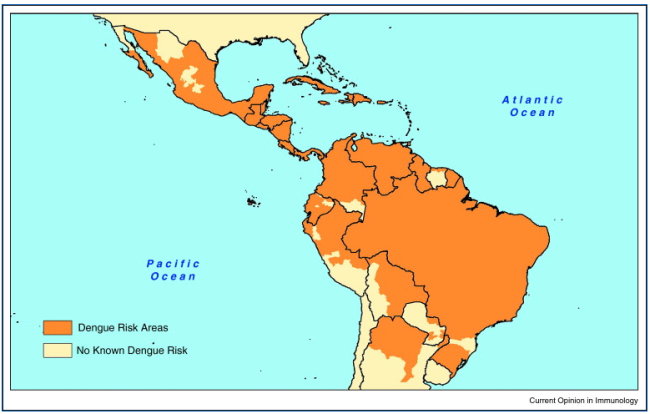
登革熱疫苗的開發工作於最近10年展開,過去進展緩慢,主要是因為登革熱疫苗開發面臨多種挑戰。包括:
- 針對類似的黃病毒疾病,如黃熱病,科學家已可研製出單價疫苗(Monovalent vaccines)。但是登革熱疫苗必須同時採用多種流行的病毒血清型(同時具有4個血清型),成為具備四價(tetravalent)的疫苗,才有可能提供持久保護。但也
就因為一次必須處理4個標的,而非只針對1個登革病毒血清型,大大提高了登革熱疫苗研製的複雜度。
- 這種四價疫苗所引發的免疫反應必須均衡且持久。如果無法確定所有4型的免疫反應均衡且持久,可能的風險是,施打疫苗的民眾對某血清型產生免疫反應後卻對其他血清型欠缺保護力。
- 科學家對預防登革熱誘發免疫保護機制沒有很好的瞭解。這讓評估疫苗所誘發的免疫反應成為一項艱鉅的工作,因為科學家如何證明四價疫苗的每一個免疫原(immunogens)都可誘發相對的免疫力的提升,困難度頗高。
- 缺乏適當的實驗動物模式來評估登革熱疫苗是最大的障礙。過去曾運用老鼠和猴子的動物模式,但牠們沒有表現出任何類似登革熱的疾病,無法進行臨床前的評估,或是做為未來人體試驗必要的檢查項目。
- 主要的安全問題在於不同病毒血清型之間互相干擾。當4個單價減毒活性登革病毒疫苗株混合在一起想匯成一劑四價的配方,免疫反應總是偏向一個血清型而排斥其他血清型。
- 候選疫苗的評估進展到臨床試驗第3階段時--藥效試驗(efficacy trials),以高危險地區的人群為對象也是一個重大的挑戰。臨床試驗第3階段的藥效試驗還必須包括長期的安全性考量和後續風險評估,評估疫苗可能引發對登革熱病產生敏感的風險。
- 研製登革熱疫苗的瓶頸之一,在於缺乏相關的免疫保護指標。
最近,科學家運用重組DNA方法(Recombinant DNA approaches),研製登革熱疫苗有了重要進展,下表為登革熱候選疫苗進入臨床試驗的近況。最先進的產品要算賽諾菲安萬特集團疫苗部門(Sanofi Pasteur)的ChimeriVax登革熱四價疫苗,正在泰國進行實地藥效試驗(field efficacy testing),並已進入第3階段的臨床試驗。這些發展中的疫苗技術進展簡述如下:

ChimeriVax登革熱四價疫苗
該項 ChimeriVax技術是基於4個重組病毒,含有從4種登革熱病毒型每一型插入到黃熱病病毒(YFV)17D疫苗株的骨幹所產生的prM和E基因。從第1期和第2期臨床試驗的結果顯ChimeriVax登革熱四價疫苗具安全性與免疫原性,每隔4-6個月施打疫苗,施打共3劑後,可誘導四價病毒中和抗體反應達到77-100%。對黃熱病病毒過敏的人,該疫苗反應較為迅速、可靠、廣泛(例如施打過一兩劑後可涵蓋所有4種登革熱血清型),這顯示在登革熱流行地區使用較少而非全程的疫苗施打就可對老年人達成保護的作用。臨床研究還顯示,針對 YFV非結構蛋白和登革熱E蛋白,疫苗可誘發細胞調節免疫作用,而反應的特點是缺乏Th2型反應和對干擾素IFN –γ(而非腫瘤壞死因子TNF-α)的偏差 (bias)。
然而,主要的挑戰在於ChimeriVax登革熱四價疫苗施打3劑的問題上(如何每隔6個月打完3劑)。這個施打期程較一般疫苗來得長,恐怕會有無法遵守時間施打的問題。此外,超過12個月不完整的免疫力可能讓接種者在施打過程期間面臨更多疾病加劇的風險。因此,雖然ChimeriVax登革熱四價候選疫苗到現在為止在臨床評估上看起來頗有希望(藥效尚有待證明),似仍有改進的空間。
TV 疫苗配方
美國國家過敏和感染症病研究所(NIAID)之感染症實驗室(LID)也正在開發一個減毒活性四價疫苗,類似ChimeriVax登革熱四價疫苗的作法,包含從不同類型的登革熱病毒的3'非編碼區(3'non-coding region)透過刪除 prM和E基因技術(或prM和E基因嵌合(chimerization)技術),得到重組病毒,但所使用的骨幹為已刪除的登革熱4型(DEN4Δ30),代替黃熱病病毒(YFV)17D疫苗株。該候選疫苗已進行大規模的第1期臨床試驗,特點是將4個病毒血清型作成獨立的單價疫苗,以便瞭解每一個單價疫苗個別成分的生物機制,理論上此四價的配方限制了病毒之間的干擾問題。
臨床試驗已進展到四價產品測試,以3種不同的配方進行第1期臨床試驗(TV001、TV002和TV003)。初步試驗數據顯示,比起其他四價減毒活性病毒,此四價疫苗足以提供均衡的四價反應,具有安全方面的優勢。LID已將該項刪除/嵌合技術授權給幾家登革熱流行國家的疫苗開發廠商,包括巴西的Butantan研究所、印度的生物E和Panacea生技公司、越南的VaBiotech生技公司。預期這些開發廠商在各自的國家可將此項技術產品往前推展。
其他登革熱疫苗開發
其他幾家公司和研究機構也致力於開發登革熱疫苗。
- Inviragen正在開發 DENVax,也是另一項嵌合四價減毒活性疫苗,利用減毒登革病毒2型菌株(16681- PDK53)為骨幹。DENVax目前正於美國和哥倫比亞進行第1階段的臨床試驗,評估皮下和皮內注射方式。
- 默克藥廠正在開發以重組亞基蛋白為基礎的疫苗,這原本是夏威夷生物技術公司的技術,主要包括重組4種登革熱病毒的C -端截短包膜醣蛋白(recombinant C-terminally truncated envelope glycoproteins, DEN-80E)。透過夏威夷生物技術公司,將含有DEN1-80E成分(HBV-001 D1)的單價配方,進行第1期臨床試驗。初步結果顯示該疫苗具安全性和免疫原性。這項亞基蛋白的方法設計在於避免病毒之間干擾的問題,這個問題是當今所有減毒活性病毒測試都可以觀察到的,預期提供替代機制來誘導平衡的四價反應。
- 美國海軍醫學研究中心也進行一項替代方法,一項以裸DNA為基礎的疫苗(D1ME-VR-P)已進入第一階段臨床試驗,也顯示具有良好的安全性和溫和的免疫原性。
- 許多其他研究小組正在進行各種候選疫苗的臨床前試驗,從經典的純化病毒滅活疫苗,到病毒載體產品,許多都以登革病毒套膜蛋白(Envelope domain III, EDIII)作為免疫原為研究重心。
參考資料:
- US CDC, last visited June 8, 2011.
- Challenges in making dengue vaccines, compiled by Saptarshi Chaudhuri, BioSpecturm, June 2011, last visited June 8, 2011.
- BioSpecturm,
www.BioSpectrumAsia.com, June 2011, last visited June 8, 2011.
- Dengue vaccines: progress and challengues, by Coller BA, Clements DE., PubMed.gov , 2011 Apr 20. [Epub ahead of print], Full Text Sources at Elsevier Science, last visited June 8, 2011.
《文:編輯中心陳麗秋;圖:US CDC Website;表:參考資料4》