NHRI Communications

健康知識
2008年諾貝爾化學獎簡介
Nobel Prize in Chemistry 2008
 水母的綠色螢光如何造成生命科學的革命性發展
水母的綠色螢光如何造成生命科學的革命性發展在1960年代,當日本化學家下村脩(Osamu Shimomura)開始研究具有生物螢光的水母(學名為Aequorea Victoria)時,他沒有想到其研究對科學會造成什麼樣的革新。三十年之後馬丁喬非(Martin Chalfie)利用水母的綠色螢光蛋白來幫助他研究生命的最小單元,亦即細胞。透過錢永健(Roger Y. Tsien)所發展的能發出各種顏色的蛋白質,現今科學家已經能夠研究過去無法觀察到的生物程序。
當科學家發展各種方法來幫助他們觀察一些原本是隱形的東西時,研究經常會向前躍進一大步。譬如當Anton van Leeuwenhoek在十七世紀發明了顯微鏡之後,一個新的世界被打開,科學家突然可以看到細菌、精子以及紅血球,甚至包括一些過去根本不知道存在的東西。
今年諾貝爾化學獎的研究,在科學上所造成的效果正是如此。綠色螢光蛋白(簡稱GFP)在過去這十年,為生化學家、生物學家、藥物學家以及其他的科學研究者扮演了一盞明燈的角色。這個蛋白在藍光或是紫外線的照射下會顯現出鮮明的綠色,例如它可以讓正在生長的癌症腫瘤發光;顯示阿茲海默疾病在腦部的發展狀況或是病原菌的生長。
一個GFP更有趣的運用是研究者可以追蹤一個單獨細胞內的運作。人體由數十億的細胞所組成,從當成幫浦的心肌細胞以及產生胰島素的beta細胞到摧毀不受歡迎的細菌之巨噬細胞,當研究者對細胞的型態越瞭解─亦即它如何的發展和運作─他們就越能夠發展出副作用越小的有效藥物。
要研究這種0.02毫米大小的細胞之運作絕非易事,要觀察細胞的組成元件,包括蛋白質、脂肪酸、碳水化合物以及其它的分子,超越了一般普通顯微鏡的能力。而要去追蹤一個細胞內的化學步驟是更加的困難,但是這卻是科學家必須能做到的精細層次。例如唯有當研究者瞭解細胞如何開始製造新的血管,他們才可能有機會去阻止癌症腫瘤細胞去營造取得營養以及氧氣的管路系統,如此將可以阻止它們的生長。
細胞的化學運作通常是透過蛋白質來控制,有成千上萬的各種蛋白質,各具有不同的功能,藉著將GFP連接到一個蛋白質上就可以得到重要的資訊,研究者可以探知某一個蛋白質會存在於哪些細胞中,他們可以追蹤它的移動以及觀察它與其它蛋白質的相互作用。感謝GFP的綠色光芒,科學家們現在可以在顯微鏡下追蹤一個單一的蛋白質。
下村脩釣出螢光的物質
現今GFP已成為全世界上千研究工作者的必備工具。它被發現的故事始於剛結束第二次世界大戰的日本,下村脩的求學被戰爭以及原子彈所造成的破壞所中斷,儘管如此,1955年他仍被名古屋大學的Yashimasa Hirata教授聘為助理,Hirata教授把他放在一個看似不可能的研究計畫上,就是去尋找讓一種磨碎的軟體動物(名為Cypridina)殘骸遇水會發光的原因。
將這個毫無經驗的助理放在一個如此困難的計畫上似乎是一件很奇怪的做法,另一個美國的頂尖研究群已經試了很長一段時間企圖分離這種物質,因此Hirata教授決定不將這個計畫交由攻讀博士學位的學生來做,因為他們需要有成功的結果才能畢業。
在1956年,克服萬難之後,下村脩終於得到了那個物質,那是一個比上述磨碎的軟體動物殘骸還要亮37,000倍的一個蛋白質。在發表了他的結果之後,下村脩被美國新澤西州著名的普林斯頓大學的Frank Johnson所網羅。作為一個臨別的禮物,Hirata教授見證了名古屋大學授給下村脩的博士學位,這是一個很不尋常的做法,因為他並不是一個正式註冊的博士班學生。
經過一段跨越太平洋以及美國大陸的漫長旅途,下村脩開始研究另一個會發出天然螢光的物質,這一次這個物質是來自於一種名為Aequorea Victoria的水母,它在受到刺激時週邊組織會發出綠色的光。
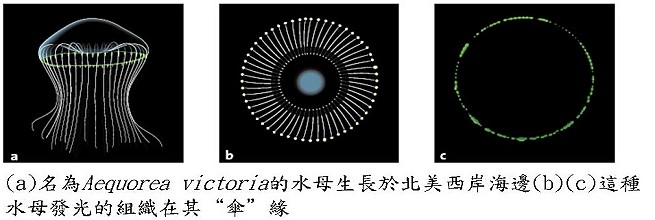
在1961年的夏天,下村脩與Johnson在北美西岸的福來德港灣(Friday Harbor)收集水母,他們切下這些水母的邊緣,並放在濾纸上擠壓而得到他們稱為“榨汁”的物質,某日下村脩將部份榨汁倒入水槽時,它發出了閃亮的光芒,因此他發現到那是因為水槽中的海水,更進一步的是海水中的鈣離子所造成的化學反應。更奇怪的是,這閃亮的光芒並非如水母邊緣所發出的綠色,而是藍色的。
Johnson與下村脩收集了整個夏天的材料,從10,000隻水母身上所得之榨汁帶回了普林斯頓,花了他們數月的時間,從所得的液體中,純化得到幾個毫克的放藍色螢光之物質,他們稱這個蛋白質為aequorin。
它在紫外線下發出綠色螢光
在他們於1962年所發表的論文中,下村脩與Johnson描述了得到aequorin的方法,他們也提到分離出一個蛋白質,它在陽光下是淡綠色的,在電燈泡下是黃色的,而且在紫外線的照射下會放出綠色的螢光,這是第一次有人描述了GFP,下村脩與Johnson稱之為綠色蛋白質,不過之後改稱之為綠色螢光蛋白質。
在1970年代,下村脩更仔細的研究了GFP的螢光,他的研究顯示GFP具有一個特殊的發色團(chromophore),亦即一種會吸光與放光的化學官能基團。當紫外線或藍色光照到這個GFP的發色團時,它會吸收光線的能量而被激發,下一刻發色團以放光的方式釋放出能量,而這個光線現在是在綠色的波長。
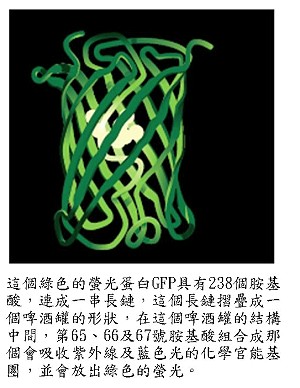
在水母中,GFP的發色團只會將aequorin放出的藍光轉換成綠光,這是為什麼水母與aequorin放射的是不同的顏色。
GFP到底有什麼革命性的重要性呢,那就是它不需要額外加入任何試劑就可以放光。相較於aequorin以及其它的生物放光蛋白質,它們都需要持續的提供一些具有高能量的分子才能放光;而GFP只需要紫外線或藍色光的照射就可發光,當光線進入細胞而碰到GFP時,它就會放出綠色光線。如果研究人員需要加入一個化學藥劑,他們需要將之注入於細胞之中,那不但將可能干擾到細胞的運作,而且在這麼微小的一個尺度下是很難執行的。
喬非有一個出色的主意
今年的第二位諾貝爾化學獎得主是馬丁喬非,他第一次聽到這個綠色螢光的蛋白質,是在1988年於一個在紐約哥倫比亞大學舉辦的學術演講中,那是有關生物放光組織的課題。當他知道有一個會發光的蛋白質時,非常的高興。
在他早先的研究中,喬非的對象是一種毫米長的蛔蟲,稱為Caenorhabditis elegans,一種世界上最常被研究的生物。雖然它僅具有959個細胞,它卻具有一個腦,它會變老也會交配。此外,這種蛔蟲的基因有三分之一是與人類的基因相關。更有甚者,C. elegans是透明的,這使得研究者能輕易的透過普通的顯微鏡來研究它的組織。
在這個1988年的學術演講中,喬非體認到這個綠色螢光的蛋白質將會是一個棒極的工具來將此蛔蟲顯像,它可以成為許多蛔蟲細胞中所進行的各種活動的一個放光信號。
如果我們真的要體會喬非的主意,我們需要知曉一些細胞生物學。如同上述,各種不同的蛋白質幾乎執行了所有細胞中的工作,而在我們的體內有成千上萬的蛋白質,雖然它們擔負了眾多不同的功能,所有的蛋白質都是用同樣的方法構築的。它們都是由二十個不同的胺基酸組合成的長鏈,它們相互之間的差異在於鏈的長度、胺基酸的序列以及結構如何的摺疊。
原則上每一個基因就是對一個蛋白質的描述,當細胞需要一個蛋白質時,那個基因就會被活化,導致細胞去合成所需的蛋白質。
譬如當你吃了一大袋甜食而你的血糖指數太高時,在胰臟的beta細胞的胰島素基因就會被開啟,所有的體內細胞都在它們的核中安全的儲存著胰島素基因,但是只有beta細胞會對高血糖有反應而開始製造胰島素,這個基因的開關,亦即啟動子(promoter)就會被打開,它在DNA上很靠近該基因的位置,當啟動子被活化之後,胰島素基因就開始被複製,那就好像在影印一本保藏在一個防火儲存櫃中的貴重舊書,當細胞需要使用並讀取基因藍圖時這一個版本是必須的。
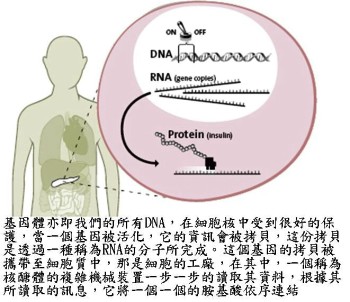
胰島素基因的拷貝從細胞核被攜帶至細胞質中,那是細胞的工廠,然後這個基因的拷貝被用來作為一個將胺基酸結合起來的設計圖而依此製造出胰島素,胰島素被釋放到血流中最後黏附到會吸收並儲存糖的肌肉及脂肪細胞。
喬非的主意是將GFP的基因連接到不同的基因開關或是其它的蛋白質之基因,他就可以觀察到細胞的基因開關被活化,而且他可以看到不同的蛋白質在何處被產生,這個綠色的光就成為了不同事件發生時的信號燈。
一個意外的發現
為了測試他的想法,喬非需要找出GFP基因在Aequorea Victoria的基因體中的位置。經過一些調查,喬非發現一位在麻州的木洞海洋研究所(Woods Hole Oceanographic Institute)的Douglas Prasher已經著手開始尋找GFP基因,喬非聯繫了Prasher並請他在成功的得到該基因時告訴他。在研究的語言上這稱為基因複製,一個研究者從一個生物的基因體中分離出一個基因,透過DNA的技術幫助,將之放入一種很容易操縱的單細胞生物中,通常研究者會使用一種稱為Escherichia coli的普通腸道細菌,他們會透過植入的基因之活化,將這種細菌轉變成一個蛋白質的製造工廠。
幾年之後,Prasher將GFP基因送給了喬非,喬非接著指導一位研究生,Ghia Euskirchen,透過一些方法企圖讓E. coli製造GFP。
約莫一個月之後,Euskirchen告訴喬非他成功了!他們可以在顯微鏡下觀察到當細菌受到紫外線的照射時會放出綠光,這個發現成就了今日GFP革命性運用的基礎,但是這個發現本身其實是相當意外的。
在1990年代初期,科學家通常假設天然的螢光分子以及顏料(賦予花朵、魚類以及一些其它生物體的顏色),是在細胞中經過數個步驟產生,每一個步驟各需要一個蛋白質來控制其化學製程。許多的專家相信有幾個不同的蛋白質需要用來產生這個GFP的發色團,但是喬非與Euskirchen的實驗顯示這個假設是錯誤的,除了GFP之外不需要任何其它的蛋白質。
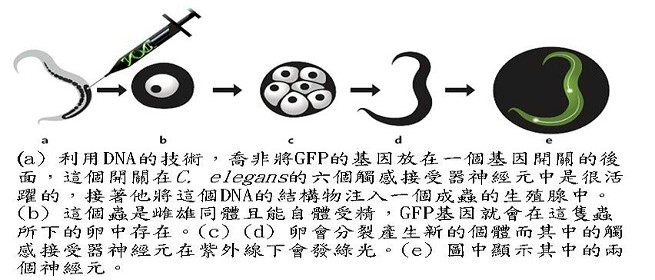
下一步,喬非將這個基因放在一個啟動子的後面,這個啟動子在C. elegans的六個觸感接受器神經元(touch receptor neuron)中是很活躍的。喬非以及合作者於1994年二月份的Science期刊上發表了這項研究成果。在這份期刊的封面,讀者可以看到一個C. elegans的影像,其中的觸感接受器神經元發散著亮綠的光芒。
錢永健創造了一個具有像彩虹般各種顏色的調色盤
現在是第三位諾貝爾化學獎得主錢永健登場的時候,他在GFP革命中的偉大貢獻在於延伸了研究工作者的調色盤,提供了許多新的顏色,延長了放光的時間並增強了亮度。
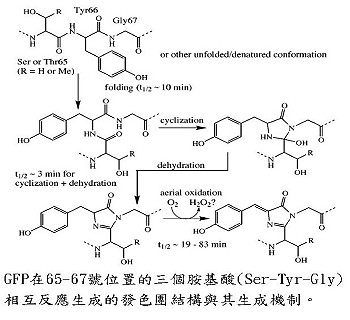
在一開始,錢永健描繪了在這238個胺基酸長度的蛋白質中的發色團是如何的透過化學的反應而產生。一些研究者在過去已發現了在65-67號位置的三個胺基酸相互的反應生成發色團,錢永健的研究則進一步的顯示這個化學反應需要氧氣,並解釋了這個反應如何在沒有其它的蛋白質幫助下發生。
藉著DNA技術的幫助,錢永健更進一步在GFP上各不同部位的胺基酸做了更換,這導致了這個蛋白質能吸收和放射不同波長的光。藉著改變胺基酸組成的實驗,錢永健發展出GFP的變體,能閃耀出更強的各種光,例如青綠色、藍色和黃色。這就使得現今的研究者能讓不同的蛋白質標記上不同顏色,來檢視它們的相互作用。
不過,一個錢永健無法讓GFP所發的光是紅色,紅光更容易穿透組織,因此對想要研究人體內的細胞和組織的研究者特別的有用。
在這個時候,Mikhail Matz與Sergei Lukyanov這兩位俄國科學家開始參與了這個GFP的革命,他們從放螢光的珊瑚中尋找與GFP相像的蛋白質,找到了六個蛋白質,其中一個是紅色的,一個是藍色的,而其餘的則是綠色。
這個想要的紅色蛋白質,DsRED,不幸的比GFP更大且更重,DsRED具有四個胺基酸鏈而非一個,較不常作為研究生物程序中的螢光標籤。錢永健的研究團隊解決了這個困難,重新設計了DsRED,使得這個新的蛋白質不但更為穩定而且只具有一條胺基酸鏈就可以發光,因此可以較容易接在其它的蛋白質上。
從這個較小的蛋白質,錢永健的研究團隊又發展了一些具有讓人垂涎名稱的蛋白質,像是mPlum、mCherry、mStrawberry、mOrange和mCitrine,這些名稱取自於它們所放射的光。幾個其它的研究者和公司也提供了這個色盤上的其它顏色。因此在下村脩第一次報導了那個綠色螢光蛋白質的46年之後,我們擁有了一個由各種類似GFP的蛋白質所組成的萬花筒,閃耀著像彩虹般的各種顏色。
腦彩虹
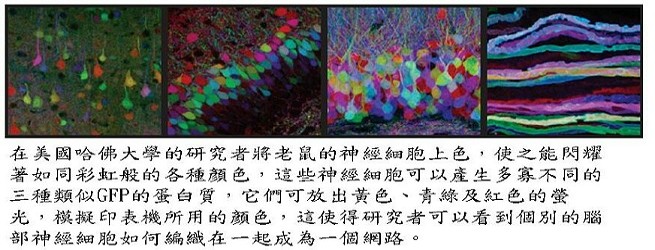
有三個這種蛋白質被研究者運用在一個極為精采的實驗中。首先將老鼠的基因做修飾使得它們腦部的神經細胞能產生多寡不同的幾種顏色,包括黃色、青綠及紅色,這幾個顏色的組合類似於電腦的彩色印表機所用的顏色,其結果就是一個老鼠的腦部閃耀著如同彩虹般的各種顏色。這些研究者因此可以追蹤在腦部濃密的網路中,某些個別細胞的神經纖維,這些研究者稱呼這個實驗為腦彩虹(the brainbow)。
砷和重金屬的GFP感測器
這個綠色螢光蛋白質也可以運用在生物技術的應用,包括在井水中砷的感測,這是在東南亞某些地區的嚴重問題,在那裡天然的砷毒害了許多人。研究者將對砷有抵抗力的細菌做基因的修飾,使得它在砷存在時會發出綠色螢光。科學家也修飾了其它的生物,當感測到具爆炸性的TNT或一些重金屬如鎘或鋅的存在時會發出綠色螢光。現在甚至於有些含GFP的玩具,能在黑暗中發光。
還有一個謎團需要解決
當下村脩開始研究海洋中具螢光的生物時,他想要瞭解為何會讓它們閃耀,這是一個典型的例子,顯示了基礎的研究如何的導致了一個科學的革命性發展。
不過一個謎團仍待解決,為什麼水母Aequorea Victoria會發光?許多海洋中的生物會使用生物螢光蛋白所發的光來迷惑它們的敵人、吸引食物或勾引伴侶,但是沒有人知道Aequorea Victoria是如何的進化而製造出aquorin以及GFP。
轉載至 http://www.ch.ntu.edu.tw/nobel/nobel97.htm
本文譯自諾貝爾化學獎委員會公佈給大眾的新聞稿:
http://nobelprize.org/nobel_prizes/chemistry/laureates/2008/info.pdf
若需要進一步的資訊,請至以下網頁點選:
http://nobelprize.org/nobel_prizes/chemistry/laureates/2008/chemadv08.pdf
《文:台灣大學化學系蔡蘊明教授譯;圖:摘錄自原文》