NHRI Communications

學術交流
國家衛生研究院個人癌症風險演講報導(一)-個人癌症風險整合預測模式
Personalized prediction model of cancer risk and clinical outcome: an integrative approach
 本院群體健康科學研究所衛生政策研究組於2009年3月18日邀請美國德州大學休士頓安德森癌症中心(MD Anderson Cancer Center)癌症預防的Betty B. Marcus Chair、流行病學教授吳息鳳博士(Dr. Xifeng Wu)與林潔博士(Dr. Jie Lin)來院進行2場演講:第一場吳博士的講題為「個人癌症風險整合預測模式(Personalized prediction model of cancer risk and clinical outcome: an integrative approach)」,第二場由林博士的講題為「吸菸相關癌症風險評估(Risk Assessment for tobacco-related cancers)」。
本院群體健康科學研究所衛生政策研究組於2009年3月18日邀請美國德州大學休士頓安德森癌症中心(MD Anderson Cancer Center)癌症預防的Betty B. Marcus Chair、流行病學教授吳息鳳博士(Dr. Xifeng Wu)與林潔博士(Dr. Jie Lin)來院進行2場演講:第一場吳博士的講題為「個人癌症風險整合預測模式(Personalized prediction model of cancer risk and clinical outcome: an integrative approach)」,第二場由林博士的講題為「吸菸相關癌症風險評估(Risk Assessment for tobacco-related cancers)」。吳教授一開始即指出流行病學研究由最初傳統蒐集問卷資料的研究方式,之後結合血清、免疫醫學等分子醫學研究,現在則更結合環境因素、遺傳因子等針對個人減少風險進行整合性的研究。除了瞭解生活習慣與整體環境對於人體的影響之外,現今之重點為預估與減少風險,期望能藉由風險預估模型提供個人化預防與早期偵測,因不同的風險程度而提供不同的改善方法,如生活方式的改變、疾病篩檢、化學藥物防癌與預防疾病的診療等。在臨床上,適藥性因人而異,沒有「一體適用(one size fits all)」的藥物,大多數的藥物對30%至70%的病患有效,且多重的因素會決定藥物的作用與反應,而在個人化治療過程中,藥物基因學則扮演了相當重要的角色;是以,除了上述的預防與偵測外,透過風險預估模型還能提供個人化藥物。吳教授目前執行多項風險預估研究計畫:例如基因易感性研究,包括肺癌、膀胱癌、腎臟細胞癌、食道癌等;口腔黏膜癌前損害之癌症風險評估研究;肺癌化學放射治療之存活率預估;含鉑藥物的化學治療與放射治療等。
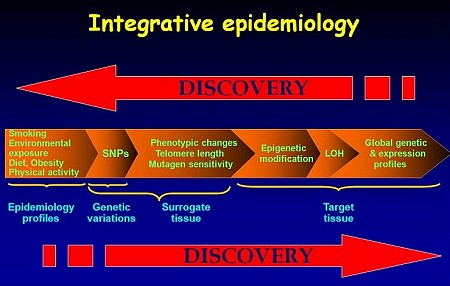 吳教授以膀胱癌研究為例,介紹整合流行病學研究。首先以病例對照研究法收集膀胱癌病例組與對照組各800例,並進行90分鐘之問卷,包括45分鐘的一般問卷與45分鐘的飲食問卷;在流行病學研究的問卷資料裡,包括抽菸狀況、飲食、職業、暴露以及家族遺傳史;樣本的蒐集包括尿液、血漿/血清、DNA、淋巴細胞與腫瘤組織等;分子化驗則包括尼古丁成癮基因、代謝多形性、突變敏感性/DNA修復能力、分子細胞生成、腫瘤微環境與甲基化等。所收集的研究樣本裡,800例膀胱癌患者並無限制病期或年齡,但皆先經過組織學確認,且尚未接受過化學治療或放射治療;而對照組則選取了與病例組相仿之年齡、性別、種族等共800例。所有的資料分為2部分,其中之50%用以發展風險模型,另50%的資料則用以確認模型之正確性。
吳教授以膀胱癌研究為例,介紹整合流行病學研究。首先以病例對照研究法收集膀胱癌病例組與對照組各800例,並進行90分鐘之問卷,包括45分鐘的一般問卷與45分鐘的飲食問卷;在流行病學研究的問卷資料裡,包括抽菸狀況、飲食、職業、暴露以及家族遺傳史;樣本的蒐集包括尿液、血漿/血清、DNA、淋巴細胞與腫瘤組織等;分子化驗則包括尼古丁成癮基因、代謝多形性、突變敏感性/DNA修復能力、分子細胞生成、腫瘤微環境與甲基化等。所收集的研究樣本裡,800例膀胱癌患者並無限制病期或年齡,但皆先經過組織學確認,且尚未接受過化學治療或放射治療;而對照組則選取了與病例組相仿之年齡、性別、種族等共800例。所有的資料分為2部分,其中之50%用以發展風險模型,另50%的資料則用以確認模型之正確性。個人化風險模型的建立要素包括:單變量分析顯著性與臨床相關性、逐步篩選變量過程、計算變異性膨脹因素以評估共線性以及分類迴歸樹(CART)分析。以流行病學模式分析抽菸、芬香族胺(Aromatic Amines)、柴油燃料廢氣、乾洗劑(鹵化的碳氫化合物)、放射性物質以及砷暴露等6項膀胱癌危險因子之後,發現癮君子(每年超過40包者)與膀胱癌有顯著相關性。以分類迴歸樹分析暴露的交互作用,並利用突變敏感性測量DNA損害/修復程度;從突變敏感性與流行病學風險因子的聯合效應分析可以得知,隨著暴露的危險因子增加,其多變項風險比之趨勢分析呈現顯著性差異;從不同的模型分析得出,以上述6項因子結合突變敏感性後之受試者工作特徵曲線(ROC curve)之鑑別能力最高,其ROC曲線下的面積可達80%,以單點移出(Leave-one Out)預測錯誤率,對照組為27.84%,病例組為28.00%,所有樣本為27.90%,顯示出此模型的預測正確性極高。
個人化風險預估模型結合了臨床、流行病學與基因變數等因素建構而成,預期能提供最適合個人化癌症治療的方式。吳教授最後為個人化醫療提供了註解:個人化的治療與預防即是在正確的時間以正確的藥物提供正確的劑量給予正確的病患對的指示。
《文:吳息鳳教授演講;編輯中心陳筱蕾整理;審校:吳息鳳教授/溫啟邦研究員;圖:編輯中心攝於會場,左起林潔博士、吳息鳳教授、溫啟邦研究員》