NHRI Communications

研究發展
磁振造影顯影對比劑奈米粒子於活體內幹細胞的追蹤與應用
NHRI team applies MRI contrast agent nanoparticles to in vivo tracking of therapeutic stem cells
 本院奈米醫學研究中心與細胞及系統醫學研究所、台大化學系、台大醫院影像醫學部及檢驗醫學部合作,利用多種奈米粒子作為一系列幹細胞追蹤平台的研究與應用,成果已陸續發表於FASEB Journal、Nano Letters、Small、Toxicology and Applied Pharmacology及Biomaterials等國際期刊。
本院奈米醫學研究中心與細胞及系統醫學研究所、台大化學系、台大醫院影像醫學部及檢驗醫學部合作,利用多種奈米粒子作為一系列幹細胞追蹤平台的研究與應用,成果已陸續發表於FASEB Journal、Nano Letters、Small、Toxicology and Applied Pharmacology及Biomaterials等國際期刊。如何確實掌控幹細胞移植進入生物體後的分布動向,成為幹細胞治療應用成功與否的關鍵。以磁振造影顯影對比劑(imaging contrast agent,如氧化鐵或釓)所構成的奈米粒子來標定(labeling)幹細胞,再以磁振造影(magnetic resonance imaging,MRI)儀器偵測細胞內磁性訊號,是目前最有效也最適當的追蹤方法。
研究團隊在研究初期以多(中)孔性矽奈米粒子(mesoporous silica nanoparticles,MSNs)及結構為球型的「矽@氧化鐵粒子」(氧化鐵為核心,矽為外殼)標定幹細胞,結果發現這2種奈米粒子對幹細胞的磁性標定效果良好,可以利用臨床上使用的磁振造影機器在活體外及活體內偵測出幹細胞內的氧化鐵訊號,相關成果發表在FASEB Journal及Nano Letters等期刊上。
目前商品化之氧化鐵奈米粒子大多用來做細胞顯影,並只被核准用於血管注射,尚未通過細胞內的安全測試。雖然大多數研究都認為氧化鐵奈米粒子對細胞不會有毒害,但研究團隊以更嚴謹審慎的角度去分析氧化鐵奈米粒子對幹細胞的影響。研究團隊先前所研發之矽奈米粒子(MSNs與球型矽@氧化鐵粒子)雖然都能進入幹細胞進行標定,但因仍處於前期試驗階段,研究團隊2009年度先以已上市並已於臨床上使用之商品化氧化鐵奈米粒子Resovist磁振造影顯影對比劑,進行幹細胞標定的後續實驗,試驗其對幹細胞安全性,並於活體動物中建立動物模式平台,研究結果摘要如下。
一、 生物細胞安全性實驗
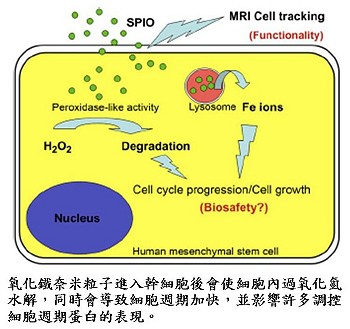
研究團隊發現Resovist不會對幹細胞造成傷害,反而會導致幹細胞的增生。Resovist加速幹細胞生長的作用機轉可能來自Resovist進入幹細胞後會使細胞內的過氧化氫水解,導致細胞週期加快,並影響許多調控細胞週期蛋白的表現。目前奈米粒子或氧化鐵奈米粒子安全性的探討,其標準未能統一且不夠嚴謹,可能因此而誤判了奈米粒子於醫學研究或應用時的適切性。此研究結果提醒了在追求奈米醫學應用發展的同時,對於生物安全性的把關是不容忽視的。這部分的結果,已發表於材料科學生物材料領域中排名第一的國際期刊Biomaterials 30:3645-3651(影響指數=6.646)。
研究顯示,Resovist除了會使幹細胞增生外,也影響幹細胞分化成骨頭細胞(osteocytes)的能力。氧化鐵奈米粒子Resovist進入幹細胞後,會分解成鐵離子,引起細胞內訊息傳遞蛋白Wnt/β-catenin的活化,進而引起下游促進細胞轉移蛋白的表現及活性上升,使得細胞轉移而無法附著於培養皿表面,因而無法分化成骨頭細胞;另外,Resovist分解成的鐵離子也會引起細胞內某些特殊蛋白(SSX cancer/testis antigen)的表現,此蛋白質的表現已經被證明會抑制幹細胞分化及促進幹細胞轉移能力,顯示利用氧化鐵奈米粒子標定幹細胞從事活體追蹤研究時,對於幹細胞的影響應該有更嚴謹的考量。
二、 幹細胞標定顯影
研究團隊利用老鼠腦腫瘤模式,將神經膠質瘤細胞(glioma cells)植入老鼠右腦形成腫瘤後,在另一邊植入經過Resovist標定的人類幹細胞,藉由臨床磁振造影觀察到幹細胞往腫瘤所在位置移動;進一步以活體外機轉輔佐探討後發現,活體內幹細胞的移動的確是受到腦腫瘤所釋放之基質細胞衍生因子(stromal cell-derived factor,SDF)吸引所致。磁振造影結果也發現,腦右側的腫瘤因為幹細胞移轉後而變小,顯示幹細胞會抑制腦瘤細胞生長;上述結果也以組織切片方式得到證實。這是第一次在小鼠腫瘤模式中以臨床磁振造影觀察人類幹細胞的移動、作用機轉、及抗癌功能,相關部分結果已投稿於國際期刊。
《文/圖:奈米醫學研究中心黃東明助研究員》