NHRI Communications

研究發展
偵測細胞凋亡的奈米螢光探針
NHRI Investigators develop real-time monitoring of cell apoptosis by nucleus shuttles of sub-nanometer gold quantum dots
 細胞凋亡(apoptosis)是一種有計畫性的細胞死亡程序,目的是在生物個體發育過程中,維持成體環境恆定和免疫調節。細胞凋亡與癌症發生,以及多種退化性疾病,如阿茲海默症、帕金森氏症和亨廷頓舞蹈病都存在密切關係。因此,對於細胞凋亡的研究以及偵測,是許多研究積極想追求的目標。
細胞凋亡(apoptosis)是一種有計畫性的細胞死亡程序,目的是在生物個體發育過程中,維持成體環境恆定和免疫調節。細胞凋亡與癌症發生,以及多種退化性疾病,如阿茲海默症、帕金森氏症和亨廷頓舞蹈病都存在密切關係。因此,對於細胞凋亡的研究以及偵測,是許多研究積極想追求的目標。最近由本院醫學工程研究組羅履維副研究員、奈米醫學中心林淑宜助研究員及楊重熙主任的研究團隊共同研發出一套偵測早期細胞凋亡的奈米螢光探針,並將成果發表於國際期刊Journal of the American Chemical Society [SCI=8.580; Rank: 7/138 in Chemistry, Multidisciplinary]。
本研究使用之奈米材料為數個金原子組成的金量子點(gold quantum dots),具有自體發光效應(photoluminescence)、極佳的抗光解穩定度(photostability)等特性,並證實對生物體不具毒性。對於開發此高量子效率之金量子點技術,已在先前發表於Chemical Communications 2008, 39: 4762–4764,並獲得美國專利暫時申請案(provisional patent application)(案號:61/086,614)。利用此一會產生自體螢光的金量子點,再加以修飾上調控物質進出細胞核的蛋白序列:出核訊號蛋白(nuclear export signal, NES)、入核訊號蛋白(nuclear localization signal),以及細胞凋亡相關酵素Caspase-3之受質DEVD 序列,即可建立功能性之奈米螢光探針,對細胞凋亡進行動態性的監測。
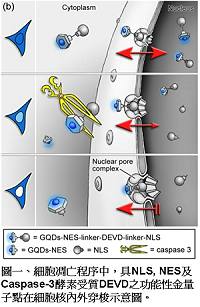
 由於此金量子點具有分子量小、穩定發光的特性,使得此具有功能性的金量子點,可用來模擬細胞中蛋白穿梭於細胞核的現象,尤其是在細胞凋亡的訊號傳遞過程,藉由觀察酵素調控此功能性金量子點在細胞核內外的穿梭程度,可用來做為一個動態的細胞凋亡探針(詳細示意如圖一所示)。
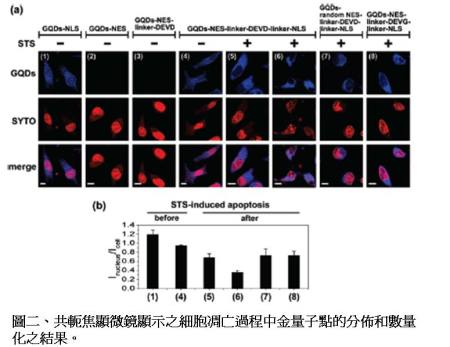
由於此金量子點具有分子量小、穩定發光的特性,使得此具有功能性的金量子點,可用來模擬細胞中蛋白穿梭於細胞核的現象,尤其是在細胞凋亡的訊號傳遞過程,藉由觀察酵素調控此功能性金量子點在細胞核內外的穿梭程度,可用來做為一個動態的細胞凋亡探針(詳細示意如圖一所示)。實驗結果顯示,當細胞受到外在物質刺激,啟動細胞凋亡路徑的同時,會引發Caspase-3酵素切割DEVD序列,使得原本藉由DEVD連結的出核訊號蛋白(NES)和入核訊號蛋白(NLS)分開,造成此金量子點在細胞裡的分佈發生變化,並且可利用金量子點在細胞核和細胞質的比例不同,來評斷細胞凋亡的程度(如圖二所示)。
因此,在發展出這樣的一個具有功能性之金量子點,可用來做為偵測細胞凋亡的即時動態探針,期待未來可應用在臨床醫學上,做為藥物篩檢或相關疾病的有利工具。
《文/圖:醫學工程研究組博士生陳乃慈、羅履維副研究員》