NHRI Communications

研究發展
利用適體結合之DNA二十面體奈米粒子作為抗癌藥物之載體用於癌症治療
NHRI researcher utilizes aptamer-conjugated DNA icosahedral nanoparticles as a carrier of doxorubicin for cancer therapy
 本院奈米醫學研究中心黃東明副研究員主導之國科會與本院贊助的研究計畫,發現以裝載阿黴素(doxorubicin)之適體(aptamer)連結之DNA二十面體對於表皮癌症細胞表現出有效且具特異性之毒殺功能。此研究成果已於今年發表在國際期刊ACS Nano 2011 Aug 23;5(8):6156-63(影響指數 = 9.855)。
本院奈米醫學研究中心黃東明副研究員主導之國科會與本院贊助的研究計畫,發現以裝載阿黴素(doxorubicin)之適體(aptamer)連結之DNA二十面體對於表皮癌症細胞表現出有效且具特異性之毒殺功能。此研究成果已於今年發表在國際期刊ACS Nano 2011 Aug 23;5(8):6156-63(影響指數 = 9.855)。在過去10年,有一系列的研究指出DNA不僅可用來構築二維奈米架構,亦能構築三維多面體。雖然已成功發展各式各樣關於三維DNA立體結構,諸如四面體、六面體、八面體、十二面體、二十面體等,其應用層面卻是付之闕如。黃東明博士實驗室專門研究具有高度生物相容性且具有高效率進入細胞能力之奈米粒子,並試著將這些奈米粒子運用在奈米醫學領域中。DNA本身就是一種自然存在於生物細胞的物質,而其所組成的奈米粒子,也必然是一種具備高度生物相容性且很有可能具有高效率進入細胞的能力(因為其為奈米尺寸,故很有潛力進入細胞)。而DNA的雙股螺旋鏈本身又可以讓很多抗癌藥物螯合於其中,故DNA奈米粒子更可能成為一個藥物載體。再者根據張拉整體法則,三角形與三角形之間彼此對合、拼裝而成的多面體是最堅固的,也就是說多面體的次單元如果是三角形,那麼此結構必然是比較穩固的。 DNA二十面體因其每個平面都是三角形,所以此構型是比較堅硬且不易變形的。綜合以上各點,包含DNA奈米粒子的生物相容性、高效率進入細胞的能力、藥物裝載的能力與其結構的穩定性,在在顯示DNA二十面體奈米粒子是可以運用在奈米醫學領域中。
截至目前為止,將DNA奈米粒子用於藥物裝載與細胞內藥物運送仍是一大挑戰,還沒有任何研究證明其藥物裝載的能力。為了克服目前DNA奈米粒子無法用於藥物裝載與藥物運送的問題,黃博士實驗室發展出新穎且容易執行的合成策略。研究團隊利用常用的引子(primer)序列創造了一個截然不同的五芒星(five-point-star)和適體連接的六芒星構型(aptamer conjugated six-point-star motif),用其分子間作用力來構築DNA二十面體,並以此來當作阿黴素之奈米載體。裝載阿黴素之適體連結之DNA二十面體對於表皮癌症細胞表現出有效且具特異性之毒殺功能。常用引子序列諸如T7、Sp6、CM等,可確保DNA二十面體的結構精確性。因為這些引子序列已歷經數10年的考驗,它們的專一性極高,故非專一性的作用可大大排除,因此可確保DNA二十面體順利成形。適體則類似抗體的作用,其可以專一地辨識癌症細胞上的某些特定蛋白,藉以作為一種高效率的標靶治療。
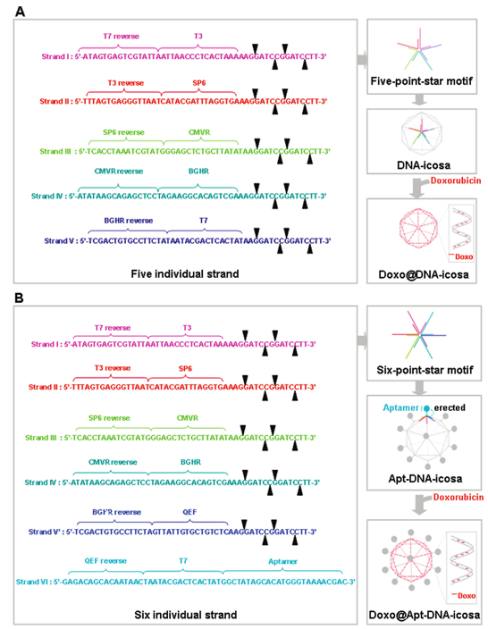
圖一:DNA二十面體之自組裝。
(A)五段單股DNA先彼此配對形成五芒星構型,而後再組裝成為DNA二十面體。(B)六段單股DNA先彼此配對形成六芒星構型,而後再組裝成為適體連結DNA二十面體。阿黴素而後螯合入此兩種DNA奈米粒子。
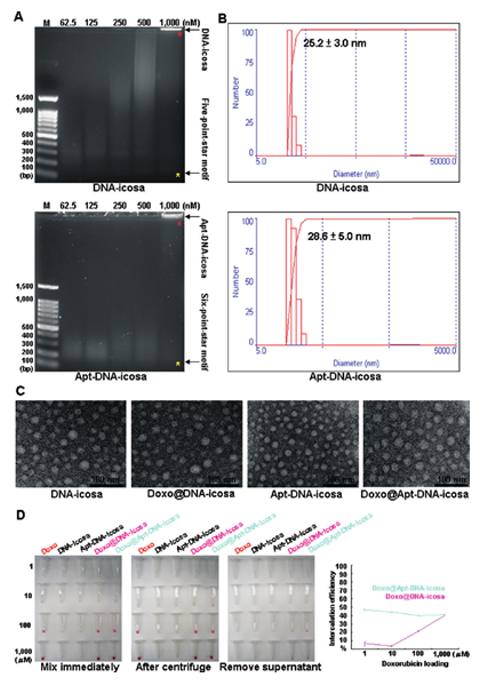
圖二:DNA二十面體與適體連結之DNA二十面體之鑑定與藥物裝載。
(A)二十面體與適體連結之DNA二十面體之電泳圖。(B)二十面體與適體連結之DNA二十面體之尺寸。(C)二十面體與適體連結之DNA二十面體之電顯圖。(D)二十面體與適體連結之DNA二十面體之藥物裝載效率。
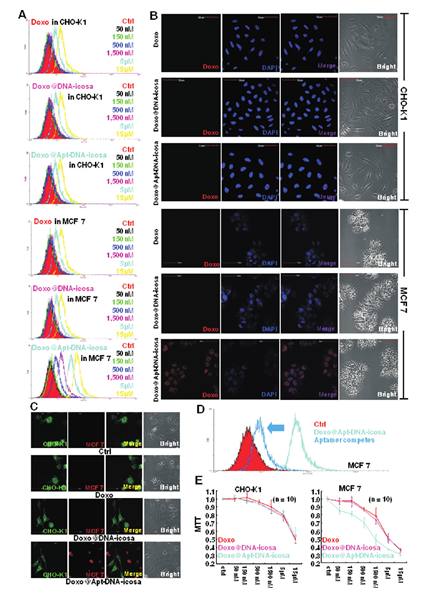
圖三:阿黴素裝載之MUC1適體連結之DNA 二十面體能有選擇性運輸至 MUC 1+ 細胞。
(A) CHO-K1 (MUC 1-)和MCF-7 (MUC 1+) 細胞以不同條件處理。流式細胞儀顯示阿黴素裝載之適體連結之DNA二十面體能有選擇性運輸至MUC 1+ 細胞。(B)共軛焦顯微鏡亦顯示阿黴素裝載之適體連結之DNA二十面體能有選擇性運輸至MUC 1+細胞。(C)CHO-K1和MCF-7細胞同時培養於同一培養皿中。共軛焦顯微鏡亦顯示阿黴素裝載之適體連結之DNA二十面體能有選擇性運輸至MUC 1+細胞。(D)競爭實驗顯示適體對MUC 1+細胞具有專一性。(E)細胞毒殺實驗顯示適體連結之DNA二十面體能有選擇性運輸至MUC 1+細胞。
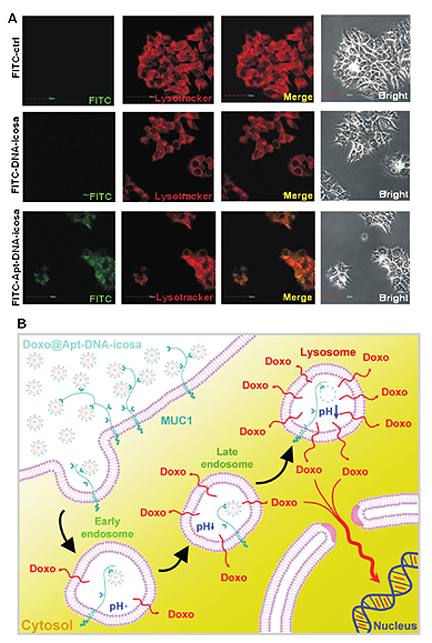
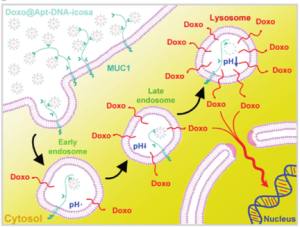
圖四:適體連結之DNA二十面體在細胞內的分布情形與細胞毒殺機制。
(A)共軛焦顯微鏡顯示適體連結之DNA二十面體有部分分布於溶脢體。(B)適體連結之DNA二十面體進入細胞途徑之假說。
綜合以上各點,裝載阿黴素之適體連結之DNA二十面體奈米粒子對於表皮癌症細胞表現出有效且具特異性之毒殺功能,未來在奈米醫學之應用將有極大之潛力。
《文/圖:奈米醫學中心黃東明副研究員》