NHRI Communications

會議報導
H5N1新型流感的流行及疫苗研發現況─ 新型流感疫苗專家會議後記
NHRI holds expert meeting on development of novel influenza vaccines
前言
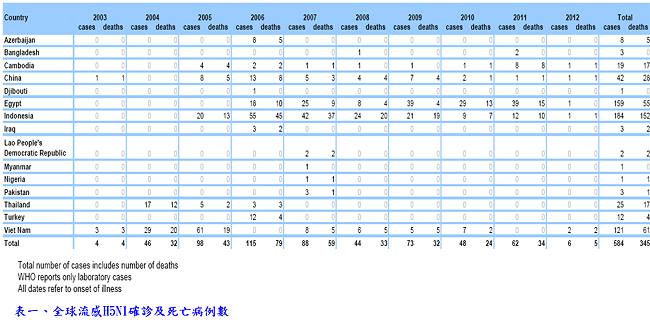
新型流感H5N1病毒於2003年起開始在東南亞地區造成人畜共通傳染,累計至2012年2月8日已在15個國家造成584病例,其中死亡病例345例,致死率高達59%,主要流行國家為印尼、埃及、越南及中國(表一)。2004年在東南亞地區造成廣泛人畜共通傳染時,引起全球恐慌,各國政府因而進行抗病毒藥物的儲備。2011年美荷兩國科學家更在實驗動物進行病毒繼代培養到第十代時證明H5N1病毒可以演變成人傳人的病毒株,震撼了學界,也引起生物安全的考量爭論。
疫苗儲備是H5N1新型流感疫情爆發時,最重要的公衛措施。世界衛生組織(WHO)於2004年委託美國及英國的參考實驗室利用基因工程開發出兩株2004年H5N1疫苗種株(A/Vietnam/1203/2004及A/Vietnam/1194/2004),並提供給想要生產H5N1疫苗的機構及廠商,衛生署疾管局於2005年4月從英國的WHO參考實驗室(NIBSC)引自疫苗種株NIBRG-14(A/VietNam/1194/2004),委託本院進行製程開發及演練生產技術,相關計畫於2011年完成;此外,2009年發生新型流感H1N1大流行,國內產官學界也開發新型流感H1N1疫苗的寶貴經驗。最近的偵測資料顯示,2004年以後在所分離出來的H5N1流感病毒,依據HA基因來分型,可區分成9種基因型(圖一)。其中以第二基因型(clade 2)最為活躍,最近在中國大陸及香港所分離出來的H5N1病毒皆為此基因型。前面所提到的2004年疫苗株是屬於第一基因型(clade 1),動物研究及疫苗臨床試驗顯示,此二基因型的抗原性不同,因此第一基因型的疫苗對第二基因型的病毒可能不具交叉保護力。為了總結歷年來台灣地區新型流感疫苗開發經驗,進而探討未來H5N1疫苗的儲備方向,本院於2012年2月11日邀請產官學專家召開此會議。共有來自產、官、學界的專家約35人,於日據時代的台北市長官邸講堂進行一天的專家會議,討論流行病學趨勢、疫苗研發、產業發展現況及政府未來的因應措施。此次會議討論十分熱烈,未來此一平台可以當作國家流感防治及疫苗發展的專家諮詢機制。

會議內容
本次會議主題包括病毒學、流行病學及疫苗研發。上午首先由農委會家畜衛生研究所鄭明珠博士介紹流感H5N1的病毒學特徵及偵測系統。禽流感病毒依其在禽類的致病力可分成高致病性及低致病性,目前已知的高致病性禽流感病毒為H5及H7亞型,低致病性H5及H7病毒有可能突變演化成高致病性。根據世界糧農組織的研究發現,高致病性禽流感H5N1病毒已在某些東南亞國家的禽類造成地方性流行(endemic),短期內不可能消失,這些國家應考慮進行疫苗接種,防止病毒繼續傳播及演化。台灣目前並未偵測到本土的H5N1流感病毒,但2003及2005年分別自走私的番鴨及金絲雀分離到高致病性H5N1流感病毒。成功大學王貞仁教授介紹新型流感H1N1(pH1N1)的病毒學特徵,此病毒為經過三次重組的豬源H1N1病毒,自2009年3月開始在墨西哥造成流行,至2009年6月已造成全球性大流行,此病毒的致病力似乎比季節性流感H1N1病毒高,並已完全取代傳統的季節性流感H1N1病毒的流行,雖然已偵測到pH1N1的抗原變異株,不過此抗原變異株尚未廣泛流行,因此,2009年的疫苗株至今仍可使用。台灣大學金傳春教授介紹新型流感H1N1及H5N1的流行病學特徵,隨著國際旅行日益頻繁,新型流感可以快速擴散,2009年pH1N1在2-3個月內傳播到全球,明顯比1968年H3N2流感大流行快;新型流感H5N1致死率高達50%以上,且流感病毒基因重組交換可能發生,因此對於新型流感H5N1的偵測不可掉以輕心,尤其是禽畜業等高危險族群。目前新型流感H5N1第2基因型(clade 2)有不少基因亞型,應密切注意中國大陸的流行狀況來選取疫苗株。台灣動物科技研究所蔡敬屏助理研究員介紹最近在美國造成豬傳人的新型豬流感H3N2病毒,此病毒的HA基因與1990年代的人流感H3N2病毒相似,因此可能只會在2000年以後出生的小孩間流行。此外,台灣豬流感病毒偵測資料顯示,台灣豬流感病毒的基因組合與美國豬流感病毒的基因組合有所不同,且有基因重組交換發生,應持續監測。
疫苗研發方面由本院李敏西博士介紹新型流感H5N1疫苗猴腎細胞(Vero cell)生產技術平台,WHO建議的H5N1流感疫苗株(NIBRG-14)是由雞胚蛋馴化過的A/H1N1疫苗種株(egg-adapted PR8 donor virus)與越南2004年H5N1病毒株利用反式基因技術(reverse genetics)重組而成,可在雞胚蛋及狗腎細胞(MDCK cell)快速繁殖,但在猴腎細胞的病毒效價低100倍,該團隊於2006-07年在猴腎細胞馴化出高成長病毒疫苗株2株,其病毒效價提高100倍,且於2009年證明此疫苗株適合在猴腎細胞微載體細胞培養系統進行大量生產,此疫苗株已獲得美國專利,具有商業價值。本院胡勇誌博士介紹新型流感H5N1疫苗狗腎細胞生產技術平台,此技術平台包括細胞庫、病毒庫、滾動瓶及生物反應器的製程,並於2011年技轉給基亞公司。中研院陳鈴津博士分享新型流感H5N1 DNA疫苗開發經驗,該團隊於2006年利用當時H5N1病毒的consensus HA基因設計第1代H5N1 DNA疫苗,此疫苗在小鼠試驗中對clade 1病毒的保護力不錯,但對clade 2病毒的保護力較差,因此於2007年又加入最新H5N1病毒的HA基因重新設計第2代H5N1 DNA疫苗,此疫苗在小鼠試驗中對clade 2病毒的保護力不錯。
中研院馬徹博士分享新型流感H1N1重組蛋白疫苗開發經驗,流感病毒HA蛋白是產生免疫力的主要抗原,HA蛋白上覆蓋不少醣分子,可能會影響保護性抗體的產生,該團隊利用哺乳類細胞生產季節性流感H1N1重組HA蛋白,經過酵素處理去除醣分子製備成HA蛋白疫苗,雪貂試驗顯示:去醣的HA蛋白疫苗比未去醣的HA蛋白疫苗產生較佳的抗體反應,且可對新型流感pH1N1產生較佳保護力。基亞公司林文理博士介紹利用可拋式生物反應器生產新型流感H1N1及H5N1疫苗的技術平台,此生物反應器是利用潮汐式細胞培養系統,具有低剪應力特色,以減低對細胞造成傷害,透過與本院合作,應用在狗腎細胞培養來生產新型流感H1N1及H5N1疫苗,目前正準備申請臨床試驗。中研院何美鄉博士分享她2009年帶領國光公司技術團隊取得新型流感H1N1疫苗上市許可的經驗,此案例成功的關鍵包括:國光公司於2000年已開始與日本北里公司合作在台灣進行季節性流感疫苗分裝並建立品管系統、參與國際聯盟迅速取得疫苗種株及相關資訊、產官學密切合作進行查廠及完成臨床試驗。國光公司張金全博士介紹該公司利用雞胚蛋開發新型流感H5N1疫苗(clade 1)的進展,目前已完成試量產(13萬顆蛋/批次),並於2011年11月提出臨床試驗申請,2012年1月取得衛生署cGMP認證。整體而言,台灣過去3年間,在流感疫苗的研發及製造上已取得重大進展。
會議最後由衛生署林奏延副署長、疾管局張峰義局長及本院感染症與疫苗研究所蘇益仁所長主持綜合討論,針對疫苗株選取及產官學合作機制進行熱烈討論,獲得以下結論:
- 目前本院、中研院及其他學研機構已無新型流感疫苗國家型群體計畫,應考慮重新啟動相關計畫。
- 可能造成人類大流行的新型流感病毒包括H2、H5、H7及H9等4種亞型,WHO也針對這些亞型分別製備疫苗種株,疾管局應取得這些疫苗種株,提供給國內相關機構進行開發,本院因有開發流感H5N1第一基因型(clade 1)疫苗的經驗,可優先考慮進行開發流感H5N1第二基因型(clade 2)疫苗。
- 開發新型流感疫苗因需考慮人畜共通傳染及高規格的生物安全,因此需跨部會的協調工作,如衛生署、農委會、國科會及國防部。
- 開發H5N1新型流感疫苗並無明確商機,政府應參考美國及日本等國家制定長期產業資助計畫。
- 2010年總統府曾召開財經諮詢小組會議,研商國內疫苗產業,責成行政院組成跨部會工作小組,衛生署林副署長將新型流感疫苗開發的議題提到此工作小組討論,盡速獲得經費補助,重新啟動新型流感疫苗國家型群體計畫,進而制定長期產業資助計畫。

《感染症與疫苗研究所李敏西副研究員、蘇益仁所長》