NHRI Communications

研究發展
嗎啡經由類鴉片受體訊息傳遞路徑調控神經細胞異源性核醣核蛋白 K的表現
NHRI researcher reports morphine drives internal ribosome entry site-mediated hnRNP K translation in neurons through opioid receptor-dependent signaling
 嗎啡(morphine)等鴉片類止痛藥是目前治療中度到重度疼痛最有效的藥物。然而,其伴隨的嚴重副作用也限制了臨床上的運用。因此,詳細研究嗎啡所媒介的細胞分子機轉將有助於釐清其止痛效果及副作用的成因。本院生技與藥物研究所葉修華助研究員實驗室研究參與嗎啡止痛效果的因子,發現嗎啡可經由鴉片受體 (MOR)促使異源性核醣核蛋白K(hnRNP K)表現量增加,進而調控疼痛閾值 (pain thresholds)。研究結果已發表於國際期刊Nucleic Acids Research。
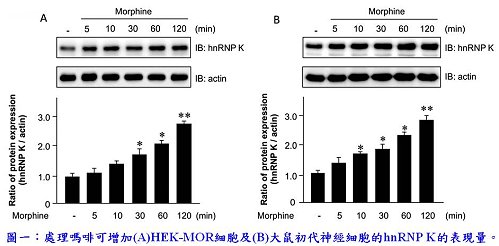
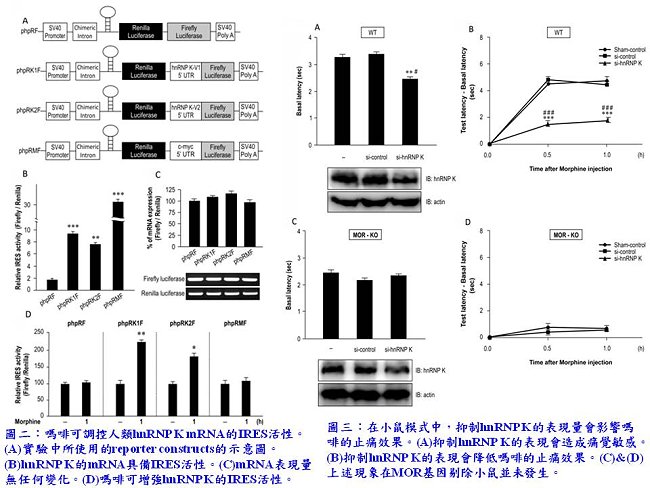
嗎啡(morphine)等鴉片類止痛藥是目前治療中度到重度疼痛最有效的藥物。然而,其伴隨的嚴重副作用也限制了臨床上的運用。因此,詳細研究嗎啡所媒介的細胞分子機轉將有助於釐清其止痛效果及副作用的成因。本院生技與藥物研究所葉修華助研究員實驗室研究參與嗎啡止痛效果的因子,發現嗎啡可經由鴉片受體 (MOR)促使異源性核醣核蛋白K(hnRNP K)表現量增加,進而調控疼痛閾值 (pain thresholds)。研究結果已發表於國際期刊Nucleic Acids Research。異源性核醣核蛋白K(hnRNP K)具有多種功能,可與MOR基因的啟動子結合進而調節轉錄活性。但關於hnRNP K是如何藉由此特性影響嗎啡的止痛效果仍是未知。研究發現,不論在新生鼠大腦初代皮質細胞(primary cortical neuron)或是表現MOR的人類胚胎腎臟細胞株(HEK293-MOR)細胞上,經由嗎啡處理後,皆可藉由活化MOR來增加hnRNP K蛋白質的表現量,但不影響其mRNA的表現量(圖一)。從bicistronic reporter assay中更進一步瞭解嗎啡會經由影響其轉譯作用來調控hnRNP K的表現量。另外,研究團隊也發現在hnRNP K五端非轉譯區 (5’UTR)具有內核醣體進入位點(internal ribosome entry site, IRES),嗎啡可促進hnRNP K的IRES活性並增加其蛋白質表現量(圖二)。此實驗結果顯示,嗎啡透過調控hnRNP K轉譯作用促使其表現量的增加,可能與嗎啡在中樞神經系統的止痛效果相關。研究團隊利用siRNA抑制hnRNP K表現後會降低嗎啡在AtT20細胞引起的膜電位過極化現象。動物實驗中,在野生型(wild type)小鼠脊椎部位抑制hnRNP K表現量會增加小鼠對疼痛的敏感度,而此現象在MOR基因剔除小鼠中並未發生(圖三)。研究結果顯示嗎啡會經由活化MOR訊息傳遞路徑調控hnRNP K的轉譯作用,進而影響其止痛效果。
《文/圖:生技與藥物研究所葉修華助研究員》