NHRI Communications

研究發展
本院成功建立斑馬魚藥物篩選平台進行抗肝癌小分子化合物篩選
NHRI researchers successfully establish zebrafish drug screening platform for small molecular compounds against liver cancer
 疾病研究和新藥開發都會使用各種動物實驗,傳統上以小鼠等哺乳類動物進行,然而昂貴的研究飼育設備及費用、以月甚至年來計算的動物生命週期,使得此類研究有其相當的困難度。有別於大小鼠,斑馬魚飼養簡單且生育能力強,經由體外受精、體外發育,一隻雌性斑馬魚每次配對最多可產下數百顆卵,且胚胎透明,並可在3天內發育完全,大大提高觀察容易度。幼魚出生3個月後即達到性成熟,繼代快且成本低。斑馬魚的基因與人類相似度高達87%,對於研究人類的疾病或相關機制都將有非常大的幫助,因此,斑馬魚可進一步作為人類疾病研究的動物模式。根據衛生福利部公布的國人十大死因,癌症連續30年居首,而肝癌在十大癌症死因排名第二,目前治療肝癌的主要方法包括手術切除、局部消融、血管栓塞甚至肝臟移植等,術後復發比率極高,但目前卻沒有針對肝癌有效的標靶藥物或化學療法。蕾莎瓦(Nexavar,學名sorafenib)是目前唯一被美國食品藥物管理局(FDA)核准的標靶藥物,用來治療晚期肝癌,可以抑制癌細胞成長且延長患者的壽命,但非適用全部患者,且其他治療肝癌的藥物成效不彰,因此迫切需要發展新的治療藥物。
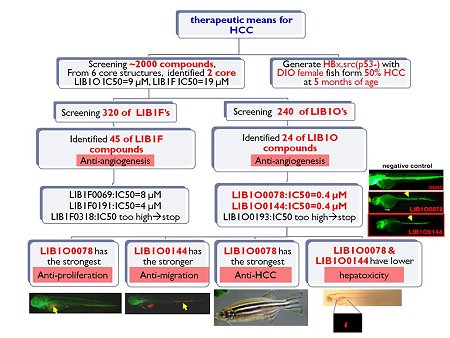
疾病研究和新藥開發都會使用各種動物實驗,傳統上以小鼠等哺乳類動物進行,然而昂貴的研究飼育設備及費用、以月甚至年來計算的動物生命週期,使得此類研究有其相當的困難度。有別於大小鼠,斑馬魚飼養簡單且生育能力強,經由體外受精、體外發育,一隻雌性斑馬魚每次配對最多可產下數百顆卵,且胚胎透明,並可在3天內發育完全,大大提高觀察容易度。幼魚出生3個月後即達到性成熟,繼代快且成本低。斑馬魚的基因與人類相似度高達87%,對於研究人類的疾病或相關機制都將有非常大的幫助,因此,斑馬魚可進一步作為人類疾病研究的動物模式。根據衛生福利部公布的國人十大死因,癌症連續30年居首,而肝癌在十大癌症死因排名第二,目前治療肝癌的主要方法包括手術切除、局部消融、血管栓塞甚至肝臟移植等,術後復發比率極高,但目前卻沒有針對肝癌有效的標靶藥物或化學療法。蕾莎瓦(Nexavar,學名sorafenib)是目前唯一被美國食品藥物管理局(FDA)核准的標靶藥物,用來治療晚期肝癌,可以抑制癌細胞成長且延長患者的壽命,但非適用全部患者,且其他治療肝癌的藥物成效不彰,因此迫切需要發展新的治療藥物。由於血管新生是腫瘤生長的必經過程,理論上若能適時抑制血管新生,應能抑制腫瘤的生長。根據這項理論,目前醫學上發展出一種抗癌的新策略,稱為「抗血管新生療法」。新生血管抑制劑治療癌症的理論近來被稱之為本世紀治療癌症的新曙光,蕾莎瓦的其中一個功能就是抑制血管新生。本院分子與基因醫學研究所喻秋華研究員研究團隊建立全套式斑馬魚藥物篩選平台,利用血管螢光魚胚胎篩選來自本院生技與藥物研究所提供的2,000種化學合成小分子,找出具抗血管新生作用的小分子藥物,發現其中兩種小分子藥物(LIB1O0078及LIB1O0144)具有最強的抗血管新生作用。此乃第一階段:快速篩選具抗血管作用的化合物。
先前研究發現,將人類腫瘤細胞異種移植注入到斑馬魚胚胎後,腫瘤細胞在斑馬魚胚胎的增殖及轉移的行為和在人類患者很類似,腫瘤細胞異種移植斑馬魚模式,篩選能抑制腫瘤細胞生長及轉移的藥物,已成為另一個快速篩選抗癌藥物的方式。喻博士研究團隊接著測試LIB1O0078及LIB1O0144這兩種化合物抑制癌細胞增生及轉移的能力,發現它們都與蕾莎瓦一樣可抑制癌細胞增生及轉移,且LIB1O0078具有較佳抑制癌細胞增生的能力,而LIB1O0144抑制癌細胞轉移的能力較好。此乃第二階段:快速驗證篩選化合物具有抗腫瘤細胞生長及轉移的能力。接著,喻博士研究團隊利用HBx,src(p53-)三重轉殖基因魚過度餵食8週,在5個月產生肝癌之動物模式,並眼窩注射藥物4週,比較LIB1O0078、LIB1O0144與蕾莎瓦,發現LIB1O0078具有最強的抗肝癌的能力,而LIB1O0144抗肝癌效果不如LIB1O0078,但二者都比蕾莎瓦更具療效。此乃第三階段:在成魚測試篩選化合物的抗癌藥效。
一般而言,小分子抗癌藥物因為毒性高,固然對癌細胞具有良好藥效,但卻因缺乏標靶性,而損害到正常細胞,引起副作用。因此,喻博士研究團隊也利用肝臟紅螢光的轉基因斑馬魚胚胎做肝毒性測試,發現LIB1O0078和LIB1O0144的肝毒性比蕾莎瓦更低。另利用篩選化合物浸泡3個小時大的斑馬魚胚胎,並觀察其發育過程,也可測試其胚胎毒性;研究團隊發現LIB1O0078和蕾莎瓦造成的胚胎毒性非常類似,且比LIB1O0144具更低毒性。此乃第四階段:快速測試有抗癌效果篩選化合物的肝毒性及胚胎毒性。
喻博士研究團隊發現篩選出的化合物對肝癌生成具有療效,且比美國FDA核准的蕾莎瓦更安全;因此,綜合上述四階段證明,斑馬魚平台的確是發現抗癌新藥物的一種優異模型。研究團隊整合了斑馬魚動物模式加上本院生技與藥物研究所化學合成小分子庫之篩選驗證,建立了一系列的高通量斑馬魚藥物篩選的平台,可以為抗癌發現更加有效和安全的藥物研發技術平台,將對疾病研究和新藥開發提供可預期的產業價值。為積極增加與產業界的合作,本項全套斑馬魚高通量新藥開發技術平台也於1月13日,在本院技轉及育成中心於台灣研發型生技新藥發展協會演講廳舉辦的「2016 國家衛生研究院創新生醫技術招商說明會」中發表,期望朝產業技術化大步邁進,讓癌症患者早日得到新科技研發所帶來的幫助,進而帶動我國生技產業搶進藥物篩選市場。
《文:秘書室賴瑨萱、分子與基因醫學研究所喻秋華研究員;圖:分子與基因醫學研究所喻秋華研究員》