NHRI Communications

研究發展
葡萄糖固醇類藥物可能降低肺癌標靶治療藥物效能研究
NHRI researchers report glucocorticoids may compromise the effect of gefitinib in non-small cell lung cancer
 肺癌是目前全球發生率最高的癌症,其中約85%屬於非小細胞肺癌(non-small cell lung cancer, NSCLC);肺癌的主要治療方法包含外科手術、放射治療、化學治療與較新的標靶藥物治療。過去10年的臨床研究發現,若帶有表皮生長因子(epidermal growth factor receptor, EGFR)活動性突變的肺癌,EGFR激酶抑制劑(EGFR-TKI)能非常有效地抑制腫瘤生長,這類的藥物例如:艾瑞莎(Iressa)或得舒緩(Tarceva),目前健保已納入給付篩檢確認有EGFR突變的患者,作為第一線治療藥物;在台灣,約50%以上的肺癌患者帶有EGFR的藥物敏感性突變,能因此受惠於此類新型藥物。一般使用標靶藥物治療的患者,一旦開始使用EGFR-TKI藥物治療後,皆會持續接受藥物治療直到病情有所改變或惡化。但在過去的觀察中,使用標靶藥物治療的患者在治療一段時間後,幾乎無可避免會對原來的標靶藥物產生抗藥性,而後被迫改用化學治療藥物。所以過去的研究多著重於尋找肺癌抗標靶藥物的機轉,也確實成功找到如EGFR-T790M這類導致第一代藥物失效的抗藥性突變;因此,很多新型的EGFR-TKI藥物即針對這些抗藥基因作為標靶,除了尋找抗藥性出現的機轉,若能找到能延長現有藥物使用時間的機會,將對臨床醫師與患者提供很大的幫助。
肺癌是目前全球發生率最高的癌症,其中約85%屬於非小細胞肺癌(non-small cell lung cancer, NSCLC);肺癌的主要治療方法包含外科手術、放射治療、化學治療與較新的標靶藥物治療。過去10年的臨床研究發現,若帶有表皮生長因子(epidermal growth factor receptor, EGFR)活動性突變的肺癌,EGFR激酶抑制劑(EGFR-TKI)能非常有效地抑制腫瘤生長,這類的藥物例如:艾瑞莎(Iressa)或得舒緩(Tarceva),目前健保已納入給付篩檢確認有EGFR突變的患者,作為第一線治療藥物;在台灣,約50%以上的肺癌患者帶有EGFR的藥物敏感性突變,能因此受惠於此類新型藥物。一般使用標靶藥物治療的患者,一旦開始使用EGFR-TKI藥物治療後,皆會持續接受藥物治療直到病情有所改變或惡化。但在過去的觀察中,使用標靶藥物治療的患者在治療一段時間後,幾乎無可避免會對原來的標靶藥物產生抗藥性,而後被迫改用化學治療藥物。所以過去的研究多著重於尋找肺癌抗標靶藥物的機轉,也確實成功找到如EGFR-T790M這類導致第一代藥物失效的抗藥性突變;因此,很多新型的EGFR-TKI藥物即針對這些抗藥基因作為標靶,除了尋找抗藥性出現的機轉,若能找到能延長現有藥物使用時間的機會,將對臨床醫師與患者提供很大的幫助。臨床上,標靶藥物與傳統化學治療藥物最大的區別,除了能快速抑制特定的腫瘤細胞外,最主要的優點在於副作用相對小很多。由EGFR-TKI藥物治療產生的較常見副作用包含了皮膚搔癢紅腫、部分噁心、嘔吐問題與較嚴重的間質性肺炎發生,在這些標靶藥物產生的副作用中,只有屬於較嚴重的間質性肺炎目前建議使用口服或注射葡萄糖固醇類(glucocorticoid)藥物控制;儘管過去許多研究顯示,合併給予葡萄糖固醇類藥物對固態腫瘤(solid tumor)化學治療常常有拮抗性,使治療藥物的效果下降,但在癌症治療中,化學治療藥物實因強烈的副作用問題導致大家聞之色變,所以臨床上常同時合併使用葡萄糖固醇類藥物,幫助患者度過化學治療產生的嚴重不適。
在標靶藥物治療的患者中,至今仍無任何有關使用葡萄糖固醇類藥物的研究,因此,本院生技與藥物研究所研究團隊試圖瞭解標靶藥物治療的患者中使用葡萄糖固醇藥物的狀況,並分別以在肺癌細胞株、小鼠腫瘤模式與健保資料庫中觀察以及進行分析。結果在肺癌細胞株中的實驗即意外發現,葡萄糖固醇類藥物對EGFR-TKI標靶藥物引起的細胞凋亡現象有很強的抑制作用,原本分別對第一代與第二代EGFR-EKI藥物敏感的肺癌細胞株,在dexamethasone這類葡萄糖固醇藥物出現後,迅速地中和了標靶藥物的效果,而這個中和效果則是可以被目前常用的葡萄糖固醇受體抑制劑RU-486再次扭轉(圖1)。
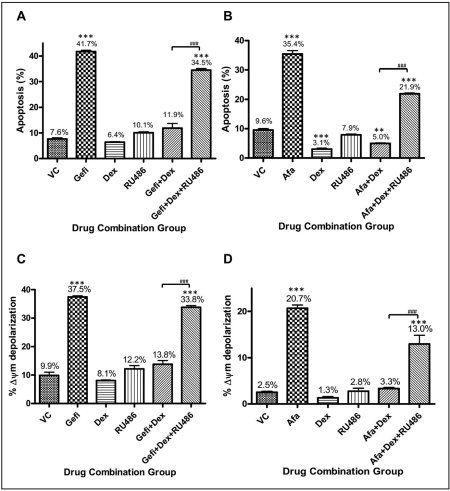
圖1. Dex藥物合併使用gefitinib對肺癌細胞毒殺效能;(A) PC9 (EGFRexon19del E746-A750) 細胞分別以控制組(DMSO)、gefitinib (200nM)、Dex(1 μM)、Ru486(1 μM)、gefitinib+Dex或gefitinib+Dex+RU486進行處理,48小時之後使用AnnexinV/PI染色與流式細胞儀偵測細胞凋亡比例;(B) NCI-H1975 (EGFRL858R/T790M) 細胞以相同於(A)的藥物處理,除了將gefitinib(200nM) 變更為afatinib(500nM),同樣於48小時之後使用AnnexinV/PI染色與流式細胞儀偵測細胞凋亡比例;(C) PC9細胞以相同於(A)的方式進行藥物處理,48小時後偵測粒線體膜電位(MMP)變化(% Δψm),反應細胞凋亡內生途徑啟動的比例;(D) NCI-H1975細胞以相同於(B)的藥物處理,48小時後偵測MMP變化,反應細胞凋亡內生途徑啟動的比例。**p<0.01 compared to VC ; ***p<0.001 compared to VC; ###p<0.001.縮寫:VC, vehicle control; Gefi, gefitinib only; Dex, dexamethasone
在此之後,使用異種腫瘤移植的小鼠模式中,也發現原來抑制腫瘤非常有效的EGFR-TKI藥物,在加入不同濃度的dexamethasone後,也迅速失去原有的藥物效能(圖2);dexamethasone明顯地抑制由藥物引發的腫瘤細胞凋亡現象。
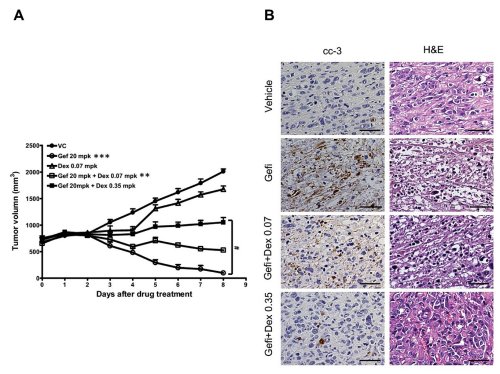
圖2. Dex抑制了gefitinib在PC9腫瘤異體移植小鼠模式中的治療效果;(A) SCID小鼠腹部皮下接種PC9 (EGFRexon19del E746-A750)細胞,當腫瘤長到800 mm3後每日連續給予口服藥物,分別為對照組(DMSO)、gefitinib(Gefi: p.o. 20 mg/kg)或合併兩種濃度Dex(p.o. 0.07 mg/kg或0.35 mg/kg),連續口服藥物10天。Data are means ± SEM. (n=4). **p<0.01 and ***p<0.001 compared to VC; #p<0.05;(B)在藥物開始投與予後第3天,犧牲小鼠取得腫瘤樣本,腫瘤凋亡的情形可由H&E染色中的核質凝聚變化與cleaved caspase 3染色(棕色)中觀察看到。Scale bars, 50 μm; cc-3, cleaved caspase 3
全民健康保險研究資料庫是台灣醫療體制中的寶庫,本研究從健保資料庫中分離收集使用艾瑞莎作為第一線治療藥物的肺癌患者,觀察合併使用葡萄糖固醇類藥物是否會對患者的預後產生影響。由於葡萄糖固醇類藥物在臨床上常用於緩和病情嚴重的患者,為了避免疾病嚴重性的干擾,研究團隊以其可能罹病的分數(propensity score,亦譯為傾向分數)進行配對,只挑選使用艾瑞莎為第一線用藥的肺癌患者,排除了較嚴重的腦轉移患者。因為腦轉移一般都會使用葡萄糖固醇藥物緩和水腫與疼痛,propensity scoring則針對患者的狀態(包含性別、年齡、糖尿病、高血壓、各種肺部急慢性疾病與是否使用氣管內管)計算分數後進行配對,產生合併使用葡萄糖固醇的實驗組患者與無合併使用葡萄糖固醇的對照組患者,這兩組在疾病的基本嚴重程度上並無差異;且為了避免因為急性需要而使用的葡萄糖固醇藥物,研究也限制了只有累積口服使用超過3個月葡萄糖固醇藥物的患者才能進入實驗組進行比較。結果發現在艾瑞莎標靶治療過程中,同時合併使用了葡萄糖固醇類藥物的患者,病情惡化的風險高很多(HR = 1.96, 1.51 – 2.54)(圖3);有超過一半只用艾瑞莎標靶治療的患者可以維持1.5年以上不惡化,而合併使用葡萄糖固醇類藥物的患者中,有一半以上在半年之內就惡化。
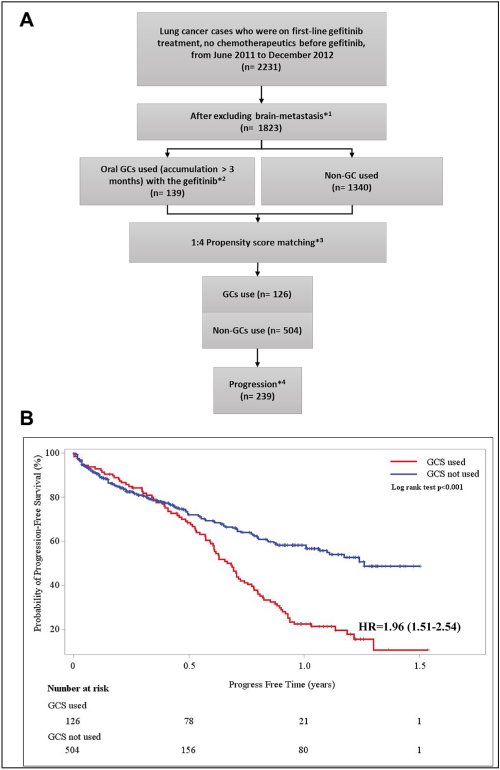 圖3. 健保資料分析流程與是否合併使用葡萄糖固醇藥物與gefitinib標靶藥物的疾病惡化分析(progression free survivals, years);(A)台灣健保資料庫分析流程圖:*1腦部轉移(ICD-9-CM 198.3)患者病人首先排除,因為葡萄糖固醇藥物是發生腦部轉移後常用的藥物;*2使用口服葡萄糖固醇類藥物(dexamethasone、methylprednisolone或prednisolone)累積超過3個月的患者(n = 139);*3與傾向分析(Propensity score)的計算項目包含:性別、年齡、糖尿病、高血壓心臟病、腎臟病、呼吸道綜合疾病(包括:慢性肺阻塞疾病、氣喘、支氣管炎等)、腫瘤轉移與是否使用氣管內插管;*4由於健保資料庫的基本特性,在本觀察中,患者疾病惡化的定義為:開始使用化學治療藥物與患者死亡;(B)利用存活分析法(Kaplan-Meier analysis)觀察gefitinib標靶藥物治療過程中,是否合併使用葡萄糖固醇藥物與疾病惡化時間先後之差別。HR則是以Cox-Proportional Hazard方法進行相對風險估計。
圖3. 健保資料分析流程與是否合併使用葡萄糖固醇藥物與gefitinib標靶藥物的疾病惡化分析(progression free survivals, years);(A)台灣健保資料庫分析流程圖:*1腦部轉移(ICD-9-CM 198.3)患者病人首先排除,因為葡萄糖固醇藥物是發生腦部轉移後常用的藥物;*2使用口服葡萄糖固醇類藥物(dexamethasone、methylprednisolone或prednisolone)累積超過3個月的患者(n = 139);*3與傾向分析(Propensity score)的計算項目包含:性別、年齡、糖尿病、高血壓心臟病、腎臟病、呼吸道綜合疾病(包括:慢性肺阻塞疾病、氣喘、支氣管炎等)、腫瘤轉移與是否使用氣管內插管;*4由於健保資料庫的基本特性,在本觀察中,患者疾病惡化的定義為:開始使用化學治療藥物與患者死亡;(B)利用存活分析法(Kaplan-Meier analysis)觀察gefitinib標靶藥物治療過程中,是否合併使用葡萄糖固醇藥物與疾病惡化時間先後之差別。HR則是以Cox-Proportional Hazard方法進行相對風險估計。合併了細胞學試驗、動物試驗與健保資料庫提供的結果,葡萄糖固醇類藥物可能會明顯干擾EGFR-TKI標靶藥物的效能。即使在治療上合併使用葡萄糖固醇類藥物並非標準治療建議,但透過健保資料初步的分析,本院研究團隊在2011年6月至2012年12月間,即看到超過25%的患者在第一天使用標靶藥物時就合併使用了口服葡萄糖固醇類藥物;因此研究團隊建議,臨床上使用標靶藥物治療肺癌患者時,除了在嚴重的腫瘤併發症或藥物副作用的情況下,應盡可能降低使用系統性給予葡萄糖固醇類藥物合併治療。此結果已發表在2016年11月Oncotarget期刊。
《文:國立交通大學分子醫學與生物工程研究所王祥宇博士生、生技與藥物研究所徐祖安研究員、群體健康科學研究所張新儀研究員 / 圖:國立交通大學分子醫學與生物工程研究所王祥宇博士生》