NHRI Communications

研究發展
微小核糖核酸-10a藉由維甲酸受體及組織蛋白去乙醯酶的互動調控血管內皮接受不同血液動力學作用時的病生理反應
NHRI researchers report microRNA-10a is crucial for endothelial response to different flow patterns via interaction of retinoid acid receptors and histone deacetylases
 本院細胞及系統醫學研究所裘正健特聘研究員及其研究團隊,近期在微小核糖核酸(microRNA, miR)參與血液動力學調控血管內皮病變反應之分子機制上,獲得重要的研究成果。此成果於2017年2月發表於國際知名的《美國國家科學院院刊(Proceedings of the National Academy of Sciences of the United States of America)》。
本院細胞及系統醫學研究所裘正健特聘研究員及其研究團隊,近期在微小核糖核酸(microRNA, miR)參與血液動力學調控血管內皮病變反應之分子機制上,獲得重要的研究成果。此成果於2017年2月發表於國際知名的《美國國家科學院院刊(Proceedings of the National Academy of Sciences of the United States of America)》。微小核糖核酸與組織蛋白去乙醯酶(histone deacetylases)目前已知為調節血管病生理的二大重要表觀遺傳分子,但是二者之間的關係目前仍然未知。此研究主要著重於釐清此二大表觀遺傳分子,在血液動力學調控血管內皮細胞病變過程中的關係。在自然生理環境中,血管內皮會接觸不同血流型態刺激,包含震盪型流體及脈衝式流體,此二種流體刺激被認為分別具有促進動脈硬化及抑制動脈硬化生成的作用。此研究發現,微小核糖核酸-10a(miR-10a)在內皮細胞受到震盪型剪力刺激時的表現量,為眾多受剪力調控的miR中的最低者,反之,在受到脈衝式剪力刺激時,其表現量相對較其他miR高。研究進一步發現,震盪型剪力及脈衝式剪力可藉由改變miR-10a的表現,調控它的直接標的—發炎轉錄因子GATA6,進而影響下游發炎分子(vascular cell adhesion molecule (VCAM)-1)的表現。研究亦發現,脈衝式剪力會誘導血管內皮內部的荷爾蒙受體—維甲酸受體α(retinoid acid receptor-α)與視黄醇類X受體α(retinoid X receptor-α)大量表現,以及互相結合聚集於細胞核內。維甲酸受體α及視黄醇類X受體α分別可扮演主導者以及協助者的角色,促使維甲酸受體α結合到RA反應元件(RA responsive element, RARE)上,促進miR-10a大量表現,抑制發炎訊息GATA6/VCAM-1。反之,震盪型剪力可誘導第3、5、7型組織蛋白去乙醯酶結合至維甲酸受體α,抑制miR-10a相關訊息。此外,亦發現重要的抗發炎轉錄因子Krüppel-like factor 2可藉由調節維甲酸受體α結合到RA反應元件的能力,影響下游發炎訊息GATA6/VCAM-1。研究團隊進一步將大鼠主動脈弓及腹腔動脈取下,進行體內實驗以驗證體外實驗結果;在動脈硬化生成的ApoE缺損鼠動物模式中,送入以invivofectamine試劑包覆的miR-10a,結果發現可以抑制動脈硬化生成(圖1)
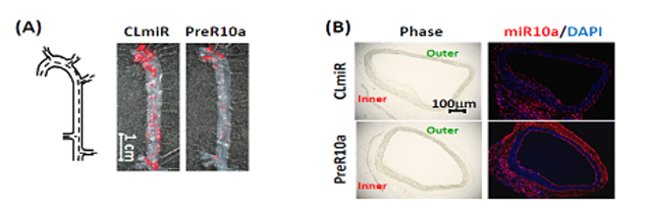
圖1:體內送入invivofectamine試劑包覆的miR-10a可以抑制動脈硬化生成。左圖:將ApoE缺損鼠血管以Oil Red染色,比較體內送入對照組miR(CLmiR)與PreR-10a對動脈硬化生成的差異;右圖;螢光定位染色證實體內送入invivofectamine試劑包覆的PreR-10a可以誘導血管壁大量表現miR-10a(紅色螢光)。
此項研究成果闡明了荷爾蒙受體—維甲酸受體α在血管內皮中扮演重要的關鍵角色,能藉由調控miR-10a/GATA6/VCAM-1訊息傳導途徑,調節不同血流剪力刺激所啟動的抗發炎及發炎訊息。而第3、5、7型組織蛋白去乙醯酶與視黄醇類X受體α可分別受到震盪型及脈衝式剪力所活化,扮演「抑制者」及「促進者」的角色,並結合至維甲酸受體α,影響其結合到RA反應元件的能力,進而調控miR-10a的表現及下游發炎訊息。以上成果對於miR與組織蛋白去乙醯酶兩大重要表觀遺傳分子與不同荷爾蒙受體之間的關係,提供新的觀點,並清楚說明了這些嶄新分子在血液動力學誘導動脈硬化過程中,所扮演的新穎機制(圖2)。
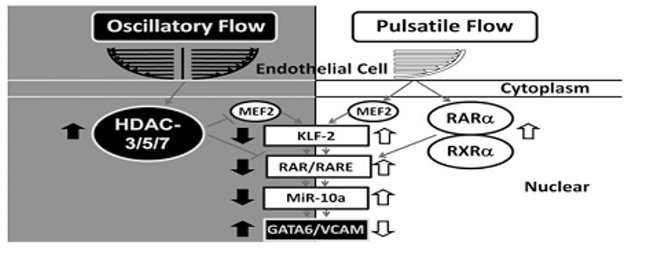
圖2:荷爾蒙受體及組織蛋白去乙醯酶在血液動力學調控血管內皮功能與病變中所扮演的角色。黑色背景分子代表促進動脈硬化訊息分子;白色背景分子代表抑制動脈硬化訊息分子
《文/圖:細胞及系統醫學研究所李定宇助理研究學者、裘正健特聘研究員》